Lesão Renal Aguda (LRA) no Adulto
CID-10: N17 – Insuficiência renal aguda
Introdução
A lesão renal aguda (LRA) é uma síndrome clínica comum, heterogênea e multifatorial, caracterizada por redução súbita e frequentemente reversível da função renal, mensurada pelo aumento da creatinina sérica e/ou pela queda do débito urinário. [1][2][4]
Anteriormente denominada insuficiência renal aguda, a LRA integra o espectro mais amplo das doenças renais agudas (DRA) e está associada a aumento expressivo da morbimortalidade em curto e longo prazo, incluindo progressão para doença renal crônica (DRC). [1][4][5]
A LRA acomete 10–15% dos pacientes hospitalizados e mais de 50% dos pacientes em unidade de terapia intensiva (UTI). [1][4] Estimativas globais apontam incidência combinada de 22% em adultos e 34% em crianças entre estudos que aplicaram a definição KDIGO em ambiente hospitalar. [1]
A incidência é maior em países de baixa e média renda, onde doenças endêmicas, contaminação hídrica e fatores socioculturais desempenham papel relevante. [1]
A LRA adquirida na comunidade responde por aproximadamente o dobro dos casos hospitalares (4,3% vs. 2,1% das internações), cursando com maior gravidade, porém com melhor sobrevida. [4]
Entre pacientes internados em UTI cardíaca, a prevalência de LRA varia de 25% a 50%, com até um terço apresentando LRA grave. [6]
O número de hospitalizações com diagnóstico principal de LRA nos EUA quase dobrou entre 2005 e 2014, passando de 281.500 para 504.600 internações. [3]
A incidência crescente da LRA reflete o envelhecimento populacional, o aumento de comorbidades predisponentes, a maior utilização de agentes nefrotóxicos e a realização de procedimentos invasivos de alta complexidade. [4]
Definição e Estadiamento
Critérios KDIGO
Em 2012, o Kidney Disease: Improving Global Outcomes (KDIGO) estabeleceu a definição harmonizada e o sistema de estadiamento da LRA, amplamente adotados na prática clínica, pesquisa e saúde pública. [1][2][3][5]
LRA é definida pela presença de qualquer um dos seguintes critérios: [1][2]
Aumento da creatinina sérica ≥ 0,3 mg/dL (≥ 26,5 μmol/L) em 48 horas
Aumento da creatinina sérica para ≥ 1,5 vezes o valor basal nos 7 dias anteriores
Débito urinário < 0,5 mL/kg/h por pelo menos 6 horas
Estadiamento KDIGO: [1][3]
Estágio 1: creatinina 1,5–1,9× basal em 7 dias ou aumento ≥ 0,3 mg/dL em 48h; ou débito urinário < 0,5 mL/kg/h por 6–12h
Estágio 2: creatinina 2,0–2,9× basal; ou débito urinário < 0,5 mL/kg/h por ≥ 12h
Estágio 3: creatinina ≥ 3,0× basal, ou ≥ 4,0 mg/dL (≥ 353,6 μmol/L), ou início de TRS; ou débito urinário < 0,3 mL/kg/h por ≥ 24h, ou anúria ≥ 12h
Em pacientes < 18 anos: inclui queda da TFGe para < 35 mL/min/1,73 m²
Observação:
O uso conjunto dos critérios de débito urinário e creatinina melhora a sensibilidade diagnóstica e refina a estimativa de risco para TRS e mortalidade. Pacientes que preenchem ambos os critérios apresentam o maior risco de morte. [1][5]
Sistemas RIFLE e AKIN
Anteriores ao KDIGO, os sistemas RIFLE e AKIN foram marcos históricos na padronização diagnóstica da LRA: [2][5]
RIFLE (ADQI, 2004): define três níveis de lesão — Risco, Lesão e Falência — e dois desfechos renais — Perda (> 4 semanas) e DRET (> 3 meses)
AKIN: incorporou aumento absoluto de creatinina ≥ 0,3 mg/dL em 48h ao estágio 1 e eliminou as categorias de desfecho; propõe três estágios com os seguintes limiares: [7]
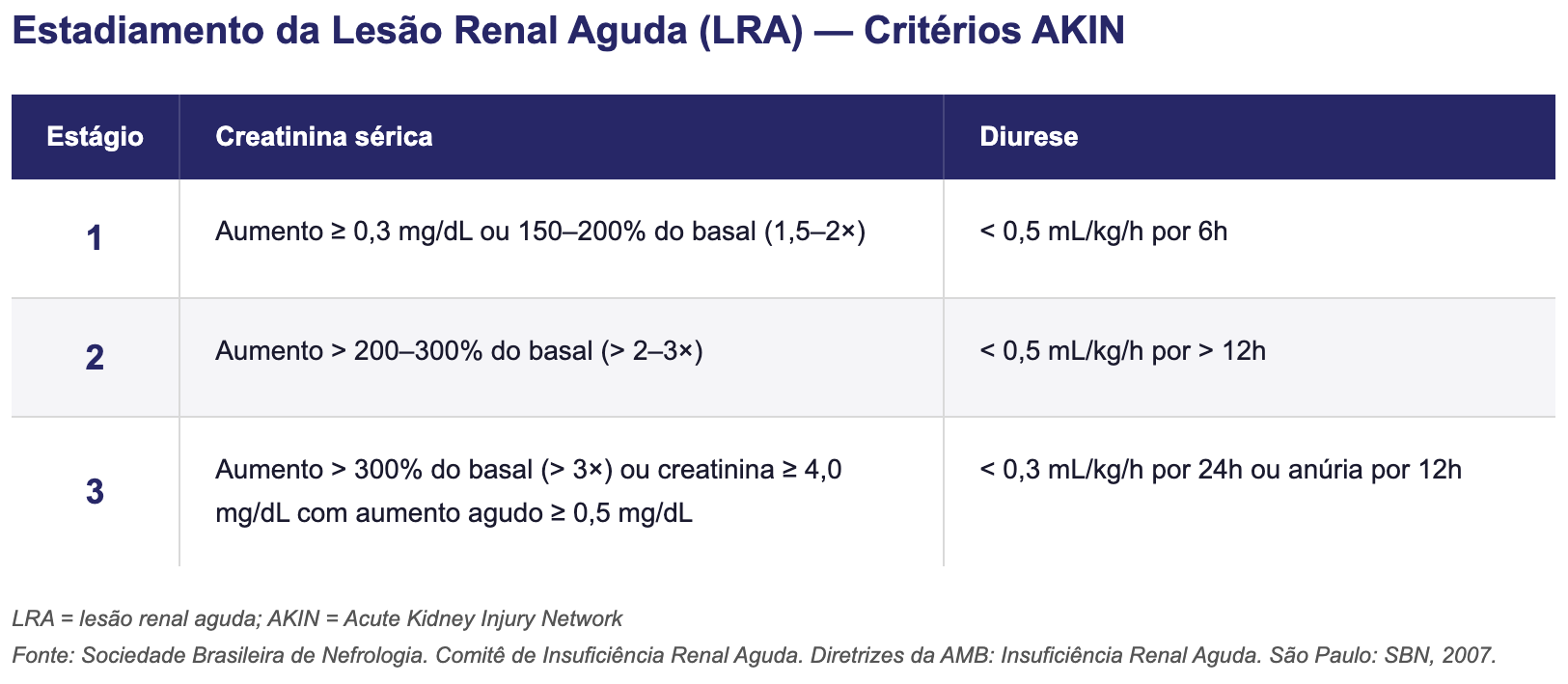
Apenas um dos critérios (creatinina ou diurese) é necessário para inclusão no estágio; pacientes que necessitem de diálise são considerados estágio 3 independentemente do estágio inicial [7]
KDIGO: combinou RIFLE e AKIN, adicionando marcos temporais mais precisos; na ausência de creatinina basal, recomenda-se usar creatinina correspondente a TFGe de 75 mL/min/1,73 m² pela equação MDRD [2][5]
Os três sistemas apresentam capacidade preditiva semelhante para mortalidade intra-hospitalar [2]
Estadiamento Ampliado com Biomarcadores (ADQI 2020)
O painel ADQI propõe refinamento do estadiamento incorporando biomarcadores de lesão estrutural ao critério funcional, permitindo identificar LRA subclínica e estratificar melhor os estágios 1, 2 e 3: [8]
Estágio 1S: biomarcador positivo sem aumento de creatinina e sem redução do débito urinário — identifica dano estrutural sem disfunção funcional detectável (LRA subclínica)
Estágio 1A: critérios funcionais presentes (creatinina/diurese), biomarcador negativo
Estágio 1B: critérios funcionais presentes, biomarcador positivo
Estágios 2A/2B e 3A/3B: mesma lógica de subdivisão por positividade ou negatividade do biomarcador de dano
Pacientes com TIMP-2 × IGFBP7 > 2,0 (ng/mL)²/1.000 apresentaram riscos associados equivalentes à progressão da LRA, mesmo sem progressão detectada pelos critérios funcionais de creatinina e débito urinário [8]
Pacientes com estágio 1S apresentam risco aumentado de progressão e necessidade de TRS em relação a pacientes sem alterações funcionais ou estruturais [8]
Doença Renal Aguda (DRA)
O KDIGO inseriu a LRA no espectro mais amplo da DRA, definida por: [1][5]
LRA, ou
TFG < 60 mL/min/1,73 m² por < 3 meses, ou
Queda da TFG ≥ 35% ou aumento da creatinina > 50% por < 3 meses
A DRA pode ocorrer sem LRA. Dados epidemiológicos demonstram que DRA sem LRA é mais prevalente do que DRA com LRA. Ambas estão associadas a maior risco de DRC incidente, falência renal tratada com TRS e morte. [1]
LRA Subclínica
Nos casos de LRA subclínica, há dano estrutural renal sem disfunção funcional detectável pelos critérios de creatinina ou débito urinário. [4][5]
Caracterizada por biomarcadores de lesão positivos (NGAL, KIM-1, cistatina C) na ausência de critérios KDIGO
Pacientes com NGAL positivo e creatinina negativa necessitaram de TRS 16 vezes mais frequentemente do que pacientes duplamente negativos (OR 16,4; IC 95% 3,6–76,9) [5]
Representa janela de oportunidade para intervenção precoce antes da perda funcional detectável [4]
Causas mais frequentes: nefrotoxicidade, AINEs e meios de contraste iodado [4]
Etiologia
A etiologia da LRA é classicamente dividida em três categorias: Pré-renal, intrarrenal (intrínseca) e pós-renal. Na prática clínica, as causas frequentemente se sobrepõem e a LRA é majoritariamente multifatorial. [1][2][4]
1) LRA Pré-renal
Responsável por 25–60% dos casos hospitalares. [4] Resulta de hipoperfusão renal por qualquer causa, com função tubular e glomerular inicialmente preservadas. [2][3]
O mecanismo compensatório renal diante de hipoperfusão mantém a TFG inicialmente. Quando a hipoperfusão persiste ou a capacidade adaptativa é insuficiente, ocorre isquemia e morte celular tubular, caracterizando a transição para necrose tubular aguda (NTA) isquêmica. [4]
A síndrome cardiorrenal tipo 1 merece destaque: piora aguda da função cardíaca reduz o volume circulante efetivo e eleva a pressão venosa central, resultando em hipoperfusão renal e ativação do SRAA/sistema nervoso simpático. A hipertensão venosa renal decorrente da congestão reduz adicionalmente a perfusão glomerular. [4][6]
Depleção volêmica verdadeira:
Hemorragia, queimaduras graves
Perdas gastrointestinais: diarreia, vômitos, alto débito por ostomias
Perdas renais: diurese excessiva
Perdas cutâneas e respiratórias, terceiro espaço (pancreatite, peritonite)
Disfunção cardiopulmonar:
Choque cardiogênico, embolia pulmonar maciça, síndrome coronariana aguda
Tamponamento pericárdico, insuficiência cardíaca congestiva
Vasodilatação sistêmica:
Sepse (causa mais comum de LRA em UTI) [3], choque anafilático, choque neurogênico, cirrose
Síndrome hepatorrenal (SHR)
Alterações hemodinâmicas intrarrenais:
AINEs, IECA/BRA, inibidores da calcineurina, hipercalcemia aguda
Contraste iodado (vasoconstrição renal)
Observações clínicas para o diagnóstico de LRA pré-renal: [7]
Oligúria não é obrigatória
Idosos podem ter recuperação tardia após correção do evento; aguardar até 48h antes de reclassificar
NTA por sepse, mioglobinúria e por contraste podem ser não-oligúricas e, nos casos de oligúria, podem apresentar FENa < 1% e/ou FEU ≤ 35%
Diuréticos podem elevar a FENa na LRA pré-renal; nesses casos, preferir FEU ≤ 35%
2) LRA Intrarrenal (Intrínseca)
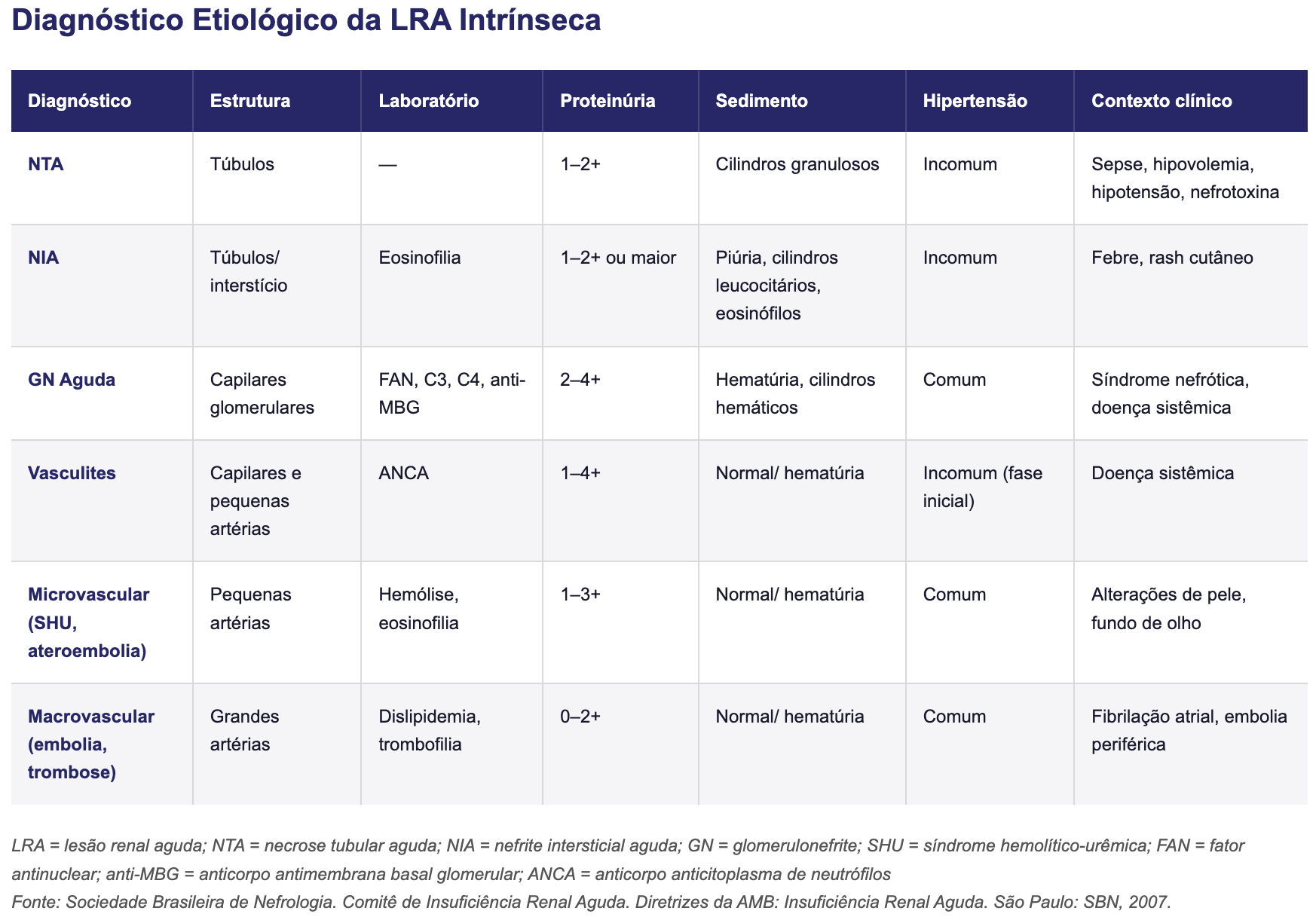
Engloba lesões das estruturas renais: túbulos, interstício, glomérulos e vasculatura. [2][3][4]
Necrose tubular aguda (NTA):
Causa mais comum de LRA intrínseca em pacientes hospitalizados (aproximadamente 45% dos casos) [2]
Etiologias isquêmicas: hipotensão grave, sepse, choque de qualquer natureza
Nefrotoxinas endógenas: mioglobina (rabdomiólise), hemoglobina (hemólise intravascular), cadeias leves de imunoglobulinas (mieloma)
Nefrotoxinas exógenas: aminoglicosídeos, vancomicina, anfotericina B, cisplatina, contraste iodado, pentamidina, tenofovir, cidofovir, foscarnet, ácido zoledrônico
Evolução em fases: iniciação (hipóxia, lesão endotelial e morte celular tubular) → manutenção (reparo celular, apoptose e proliferação) → recuperação (normalização do fluxo e homeostase intracelular) [4]
Critérios para diagnóstico de NTA séptica (associada a duas ou mais das seguintes condições de SRIS): [7]
Temperatura > 38°C ou < 36°C
Frequência cardíaca > 90 bpm
Frequência respiratória > 20 ipm
PaCO₂ < 32 mmHg
Leucócitos > 12.000 ou < 4.000/mm³
10% de bastões ou metamielócitos
Foco infeccioso documentado ou hemocultura positiva
Critérios para diagnóstico de NTA nefrotóxica: [7]
Uso de nefrotoxina em tempo suficiente
Níveis séricos nefrotóxicos precedendo a LRA
Ausência de outras causas possíveis
Reversão após suspensão da nefrotoxina; recidiva após reinstituição
Frequentemente não-oligúrica
Nefrite intersticial aguda (NIA):
Reação de hipersensibilidade tipo IV retardada, predominantemente por medicamentos [4]
Drogas mais frequentemente implicadas: IBPs, AINEs, betalactâmicos, cefalosporinas, fluoroquinolonas, rifampicina [4]
Infecções respondem por 5–10% dos casos [3]
Achado urinário característico: piúria estéril, frequentemente com cilindros leucocitários [2]
Critérios para diagnóstico de LRA por NIA: [7]
Manifestações periféricas de hipersensibilidade
Febre e rash cutâneo ou eosinofilia
Uso de droga associada a NIA (penicilinas, cefalosporinas, quinolonas, alopurinol, cimetidina, rifampicina)
Patologias frequentemente associadas: leptospirose, Legionella, sarcoidose
Confirmação por biópsia renal
Doenças glomerulares:
Representam cerca de 10% dos casos de LRA intrínseca [4]
Padrão nefrítico (glomerulonefrite proliferativa aguda ou rapidamente progressiva): mais frequentemente associado a LRA
Causas sistêmicas: nefrite lúpica difusa, vasculite ANCA, síndrome de Goodpasture, microangiopatias trombóticas (SHU/PTT), crioglobulinemia, poliarterite nodosa
Causas primárias: doença anti-MBG, GN pós-infecciosa, nefropatia por IgA, GNMP
Critérios para diagnóstico de LRA por glomerulopatia: [7]
Exame de urina com proteinúria e proteinúria > 1 g/dia
Hematúria com dismorfismo eritrocitário positivo ou cilindros hemáticos no sedimento urinário
Biópsia renal positiva
Doença vascular:
Grandes vasos: trombose ou dissecção de artéria renal, ateroembolismo (frequente após cateterismo/angioplastia)
Pequenos vasos: vasculite, microangiopatias trombóticas, hipertensão maligna
Obstrução bilateral ou de rim único funcionante é necessária para causar LRA clinicamente significativa [4]
Critérios para diagnóstico de LRA vascular: [7]
Dor lombar e hematúria macroscópica
Contexto clínico predisponente: ICC, estados de hipercoagulação, vasculites, síndrome nefrótica, evento cirúrgico precipitante
Confirmação com exame de imagem: cintilografia compatível, TC ou angiorressonância, arteriografia
Embolização por colesterol: [7]
Evento precipitante até 30 dias: manipulação de grandes vasos, cateterismo arterial, trauma
Anticoagulação, petéquias, livedo reticularis, eosinofilia, hipocomplementemia
Síndrome hepatorrenal (SHR):
Os critérios diagnósticos foram atualizados pelo International Club of Ascites (ICA) em 2015, adotando a definição KDIGO de LRA em substituição ao limiar absoluto de creatinina > 1,5 mg/dL. A atualização é relevante especialmente em cirróticos sarcopênicos, nos quais a creatinina basal é frequentemente baixa e um aumento de 0,3 mg/dL já tem significado clínico.
Critérios diagnósticos de SHR-LRA (ICA 2015): [1]
Cirrose com ascite
LRA por critérios KDIGO (aumento de creatinina ≥ 0,3 mg/dL em 48h ou ≥ 1,5× o basal em 7 dias)
Ausência de melhora após 2 dias de suspensão de diuréticos e expansão com albumina (1 g/kg/dia, máx. 100 g/dia)
Ausência de choque
Ausência de uso recente de nefrotoxinas
Ausência de sinais de lesão renal estrutural: proteinúria < 500 mg/dia, ausência de hematúria significativa, ausência de alteração à ultrassonografia
LRA associada a COVID-19:
Frequente em pacientes hospitalizados; NTA e lesão glomerular são as formas histológicas mais comuns [4]
Mecanismos: alterações hemodinâmicas, liberação de citocinas, citotoxicidade viral direta, ventilação mecânica, hipoxemia e nefrotoxinas
Achado histológico adicional: glomerulopatia colapsante (COVAN), especialmente em portadores de variantes de risco do gene APOL1 [4]
3) LRA Pós-renal
Representa 5–10% dos episódios de LRA. [4] Resulta de obstrução do fluxo urinário em qualquer nível do sistema coletor.
Exige obstrução bilateral dos ureteres, obstrução abaixo da bexiga ou obstrução de rim único funcionante para elevar a creatinina sérica [4]
Obstrução completa causa anúria; incompleta pode cursar com volumes urinários variáveis ou poliúria
Após alívio da obstrução, diurese pós-obstrutiva ocorre em até 50% dos casos, com risco de hipovolemia e distúrbios eletrolíticos graves [2]
Causas principais: [2][3][4]
Hiperplasia prostática benigna (causa mais comum em homens idosos)
Litíase renal/ureteral (principal etiologia em adultos jovens, especialmente com rim único)
Tumores pélvicos, prostáticos, vesicais, cervicais ou retroperitoneais
Bexiga neurogênica, fibrose retroperitoneal
Necrose papilar renal (AINEs)
Coágulos sanguíneos, estenose uretral
Critérios diagnósticos de LRA pós-renal: [7]
Obstrução urinária
Dilatação pielocaliceal ao exame ultrassonográfico
Diâmetro anteroposterior da pelve renal > 30 mm
Diâmetro AP da pelve > diâmetro AP do rim
Evidência clínica de iatrogenia intraoperatória
Anúria total
Fisiopatologia
A fisiopatologia da LRA é heterogênea. Diferentes etiologias de lesão renal elicitam respostas divergentes nos níveis molecular, celular e funcional, de forma simultânea ou sequencial. [1][4]
Os principais mecanismos patogênicos incluem: [1][4][6]
Disfunção microcirculatória: alteração do tônus vascular, redistribuição e déficits focais de perfusão intrarrenal
Inflamação: recrutamento de leucócitos, ativação de células inflamatórias, liberação de mediadores inflamatórios, reação imune intersticial
Disfunção endotelial: vasodilatação, aumento de permeabilidade vascular, formação de microtrombos
Toxicidade tubular direta: lesão ou morte celular aguda, feedback tubuloglomerular, parada do ciclo celular
Congestão venosa renal: compressão de veias intrarrenais, síndrome compartimental intrarrenal
Disfunção mitocondrial: disfunção da cadeia respiratória, down-regulation de processos consumidores de ATP
Obstrução: intratubular (cristais, pigmentos, cadeias leves), intraluminal ou extrínseca
Doença glomerular: microangiopatia trombótica, processos autoimunes, ativação do complemento
LRA associada à sepse: [1][4]
A sepse é a etiologia mais frequente de LRA grave em pacientes críticos, acometendo aproximadamente 70% dos pacientes sépticos e frequentemente evoluindo para estágio 3. Mecanismos específicos incluem:
Inflamação sistêmica e renal; ativação do sistema complemento
Disfunção microcirculatória com hipoperfusão e hipóxia tecidual renal
Disregulação do SRAA; disfunção mitocondrial e reprogramação metabólica
Liberação de micro-RNAs causando morte celular por repressão pós-transcricional
Ativação da efferocitose (clearance de células mortas por fagócitos) com amplificação da lesão tecidual
Quadro Clínico
As manifestações clínicas da LRA dependem da causa e do grau de comprometimento da função renal, sendo frequentemente inespecíficas e mascaradas pela doença de base. [7]
A história clínica é fundamental para estabelecer a causa subjacente (hipovolemia, drogas, contrastes radiológicos, sepse), os fatores de risco (idade, disfunção renal prévia, comorbidades) e a gravidade da LRA. [7]
Manifestações clínicas específicas são incomuns:
Febre, mal-estar, rash cutâneo e sintomas musculares ou articulares podem estar associados a nefrites intersticiais, vasculites ou glomerulonefrites [7]
Dor lombar ou suprapúbica, dificuldade de micção, cólica nefrética e hematúria podem sugerir LRA pós-renal [7]
Presença de livedo reticular e microinfartos digitais pode sugerir doença renal ateroembólica [7]
Sinais de hipovolemia e hipotensão arterial auxiliam no diagnóstico de LRA pré-renal [7]
Principais manifestações órgão-específicas: [7]
Digestivas: inapetência, náuseas, vômitos incoercíveis, sangramento digestivo
Cardiorrespiratórias: dispneia, edema, hipertensão arterial, insuficiência cardíaca, edema agudo de pulmão, arritmias, pericardite, pleurite
Neurológicas: sonolência, tremores, agitação, torpor, convulsão, coma
Hematológicas: sangramentos, anemia, distúrbios plaquetários
Imunológicas: depressão imunológica, tendência a infecções
Nutricionais: catabolismo aumentado, perda de massa muscular
Cutâneas: prurido
Classificação da LRA quanto à diurese: [7]
Anúrica total: 0–20 mL/dia
Anúrica: 20–100 mL/dia
Oligúrica: 101–400 mL/dia
Não-oligúrica: 401–1.200 mL/dia
Poliúrica: 1.201–4.000 mL/dia
Hiperpoliúrica: > 4.000 mL/dia
Avaliação Diagnóstica
História e Exame Físico
A história clínica e o exame físico são a base da avaliação etiológica da LRA. [2][3]
Pontos essenciais na história:
Eventos precipitantes: diarreia, vômitos, febre, hipotensão, sangramento
Medicamentos nefrotóxicos (AINEs, IECA/BRA, aminoglicosídeos, IBPs, contraste iodado)
Comorbidades predisponentes: DRC prévia, ICC, cirrose, DM, doença vascular periférica
Perfil do débito urinário:
Oligúria: favorece LRA em geral [2]
Anúria súbita: sugere obstrução aguda, GN grave ou oclusão vascular [2]
Poliúria: sugere defeito de concentração tubular (NIA) ou nefropatia pós-obstrutiva [2]
Sintomas sugestivos de DRC prévia: fadiga crônica, anorexia, noctúria, prurido
Exame físico direcionado: [2][3]
Sinais vitais ortostáticos: detectam hipovolemia
Pele: livedo reticularis ou infartos cutâneos (ateroembolismo/vasculite), rash maculopapular (NIA por drogas), turgor reduzido (hipovolemia), púrpura (vasculite)
Olhos/ouvidos: icterícia (hepatopatia), ceratopatia em banda (mieloma), retinopatia diabética, perda auditiva (doença de Alport)
Cardiovascular: pressão venosa jugular (volemia), atrito pericárdico (pericardite urêmica), sopro cardíaco (endocardite), pulso (estabilidade hemodinâmica)
Avaliação hemodinâmica em SCR: avaliar pressões de enchimento (congestão) e débito cardíaco (perfusão) pelo exame físico, ecocardiografia e/ou hemodinâmica invasiva [6]
Exames Laboratoriais
Séricos: [2][3]
Painel metabólico completo: creatinina, ureia, eletrólitos, bicarbonato, glicose
Gasometria arterial quando acidose é suspeita
Hemograma completo
CPK, LDH (suspeita de rabdomiólise ou hemólise)
SPEP/UPEP em idosos para exclusão de gamopatia monoclonal e mieloma múltiplo
Estimativa do RFG: [7]
Cockcroft-Gault: ClCr (mL/min) = (140 − idade) × peso / (72 × creatinina plasmática); para sexo feminino: × 0,85
Unidades: idade em anos; peso em kg; creatinina plasmática em mg/dL
MDRD simplificada (Levey): ClCr (mL/min) = 186 × Cr⁻¹,¹⁵⁴ × idade⁻⁰,²⁰³; para sexo feminino: × 0,742; para negros: × 1,21
A dosagem de creatinina é marcador pouco sensível de função renal; pacientes com creatinina < 1,5 mg/dL podem apresentar reduções significativas da TFG [7]
Urinários: [2][3]
Urina tipo 1 com sedimento: orientam etiologia (ver tabela)
Eletrólitos urinários:
Fração de excreção de sódio (FENa) < 1%: sugere causa pré-renal; > 2%: causa intrínseca
Fração de excreção de ureia (FEU) < 35%: sugere causa pré-renal; > 50%: causa intrínseca
FEU é preferível em pacientes em uso de diuréticos [3]
Razão albumina/creatinina urinária (uACR): avalia DRC e lesão glomerular
Achados no sedimento urinário e etiologias associadas: [3][5]
Cilindros granulosos escuros ("muddy brown") e células epiteliais tubulares: NTA isquêmica ou nefrotóxica
Cilindros leucocitários, piúria estéril: NIA
Cilindros eritrocitários, acantócitos: GN, vasculite
Cilindros cristalinos: nefropatia cristalina (ácido úrico, aciclovir, sulfas, indinavir)
Cilindros hialinos: azotemia pré-renal
Cilindros cerosos: DRC estabelecida
Sistemas de escore de microscopia urinária (Chawla, Perazella, Bagshaw) quantificam células epiteliais tubulares e cilindros por campo, com especificidade para NTA e correlação com a gravidade da LRA. [5]
Biomarcadores
Biomarcadores moleculares oferecem detecção precoce, estratificação prognóstica e orientação terapêutica na LRA. [1][4][5][6][8] A integração de biomarcadores de dano e funcionais à avaliação clínica melhora a acurácia diagnóstica, refina a estratificação de risco e orienta o manejo. [8]
Categorias de biomarcadores: [8]
Marcadores de estresse celular: indicam estresse que pode resolver ou progredir para dano ou alteração funcional
Marcadores de dano estrutural: proteínas liberadas pelo rim lesado, moléculas superexpressas em resposta à lesão ou proteínas filtradas/reabsorvidas/secretadas pelo rim
Marcadores funcionais: refletem alterações na filtração glomerular
Principais biomarcadores disponíveis: [1][4][5][8]
NGAL (lipocalina associada à gelatinase de neutrófilos): urinário e plasmático; aprovado pelo FDA em 2023 para predição de LRA grave em crianças; útil para distinguir NTA de SHR em cirróticos; elevação associada a maior risco de TRS e mortalidade mesmo na ausência de critérios funcionais
AUROC para predição de TRS: 0,72 (urinário) e 0,76 (sanguíneo) [8]
KIM-1 (kidney injury molecule-1): glicoproteína transmembrana produzida por células tubulares proximais; liberada na urina após dano tubular; prediz diagnóstico e progressão
TIMP-2 × IGFBP7 (NephroCheck®): marcadores de parada do ciclo celular; aprovados pelo FDA e na Europa para predição de LRA estágio 2 ou 3 nas próximas 12h em pacientes críticos de alto risco
AUROC para predição de TRS: 0,86 (IC 95% 0,79–0,93) [8]
Cutoff ≥ 0,3 (ng/mL)²/1.000: identifica alto risco; < 0,3 exclui progressão para LRA mais grave com bom valor preditivo negativo
Cutoff > 2,0 (ng/mL)²/1.000: riscos equivalentes à progressão da LRA mesmo sem alteração dos critérios funcionais [8]
CCL14 (C-C motif chemokine ligand 14): liberado por células tubulares sob estresse ou dano; prediz persistência de LRA grave [1]
Dickkopf-3 urinário: glicoproteína 38 kDa secretada sob estresse tubular; prediz LRA, disfunção renal persistente e necessidade de TRS em pós-operatório de cirurgia cardíaca; razão dickkopf-3/creatinina > 471 pg/mg associada a maior risco de disfunção renal persistente e dependência dialítica em 90 dias [8]
Cistatina C: marcador funcional de 13 kDa; independente de massa muscular e ingestão dietética; mais preciso para estimar TFG após doença crítica e em estados de baixa massa muscular [1][4]
Uso de eGFR incluindo creatinina e cistatina C em algoritmo de dosagem de vancomicina melhorou atingimento de concentrações-alvo em 22% comparado ao eGFR por creatinina isolada [8]
CXCL9 e TNF urinários: auxiliam na distinção de NIA vs. NTA e identificam pacientes que se beneficiam de corticoterapia [1]
IL-18 urinária: citocina pró-inflamatória liberada após dano tubular; útil para diagnóstico precoce e prognóstico de LRA em múltiplos cenários clínicos [5]
Proencefalina A (PENK): polipeptídio endógeno filtrado livremente; prediz progressão, LRA persistente e necessidade de TRS; aumento precede elevação da creatinina em pacientes com piora da função renal [8]
Calprotectina urinária: complexo citosólico derivado de neutrófilos e monócitos; auxilia na distinção entre LRA pré-renal e intrínseca [8]
Hepcidina (hepcidin): hormônio peptídico de 2,78 kDa produzido predominantemente em hepatócitos; filtrado livremente; avaliação de risco e predição de LRA [8]
MicroRNAs urinários e plasmáticos: > 50 microRNAs individuais expressos na LRA, especialmente em associação com inflamação, apoptose e fibrose [8]
Painéis de biomarcadores para desfechos de longo prazo: [1]
TNFR1 e TNFR2 plasmáticos, MCP-1, uromodulina e EGF urinários mensurados 3 meses após LRA: associados à progressão de DRC e eventos cardiovasculares
Recomendações do Consenso ADQI 2020 para Uso Clínico de Biomarcadores [8]
Declaração 1 (Grau B, forte): a decisão de realizar avaliação de saúde renal (KHA) deve integrar fatores do paciente e a intensidade da exposição planejada que carrega risco de LRA
Declaração 2 (Grau B, forte): o tipo de biomarcador funcional e/ou de dano a ser avaliado deve ser orientado pelos resultados da KHA de susceptibilidade à LRA
Declaração 3 (Grau A, forte): biomarcadores de dano agudo não devem ser utilizados para avaliação de risco antes de um insulto renal
Declaração 4 (Grau A, forte): recomenda-se o uso de biomarcadores validados para identificar populações para as quais intervenções preventivas demonstraram melhorar desfechos
Ensaio PrevAKI: redução de 17% na LRA com cuidados protocolados guiados por TIMP-2 × IGFBP7 após cirurgia cardíaca [8]
Ensaio BigpAK (cirurgia abdominal maior): redução de 13% em LRA estágios 2 e 3 [8]
Declaração 5 (Grau C, forte): sugere-se combinar avaliação clínica e biomarcadores validados para triar pacientes e otimizar o momento e o tipo de intervenções
Declaração 6 (Grau B, condicional): sugere-se combinar biomarcadores de dano e funcionais com informações clínicas para melhorar a acurácia diagnóstica, reconhecer os diferentes processos fisiopatológicos, discriminar a etiologia e avaliar a gravidade
Declaração 7 (Grau C, condicional): sugere-se que combinações de biomarcadores podem auxiliar no planejamento da terapia e manejo da LRA
Declaração 8 (Grau C, condicional): a inclusão de dados de biomarcadores com avaliações clínicas pode ser usada para identificar pacientes que necessitarão de TRS e facilitar o momento ideal de início
Declaração 9 (Grau C, fraco): sugere-se que novos biomarcadores podem ser usados para predição de duração e recuperação da LRA
Declaração 10 (Grau C, forte): evidências atualmente insuficientes para recomendar o uso rotineiro de novos biomarcadores para refinar o estadiamento de DRA
Declaração 11 (Grau C, forte): recomenda-se que biomarcadores preditivos de estadiamento e progressão de DRC sejam incorporados a programas de cuidado pós-LRA/DRA e à KHA
Teste de Estresse com Furosemida (FST)
O FST avalia a integridade funcional tubular (túbulo proximal e alça de Henle): [1][5][6][8]
Administração de furosemida 1 mg/kg IV (ou 1,5 mg/kg em pacientes previamente em uso de diurético)
Débito urinário < 200 mL em 2h: sensibilidade de 87% e especificidade de 84% para progressão ao estágio 3 [1]
Débito urinário < 600 mL em 6h: preditivo de necessidade de TRS em LRA estágio 3 [6]
Prediz descontinuação de TRS com AUROC = 0,84 [8]
Supera outros biomarcadores de dano estrutural quando comparados diretamente [5]
Imagem
Ultrassonografia renal: método de escolha para excluir obstrução (hidronefrose) e avaliar morfologia renal; avalia também preenchimento intravascular e congestão [1][2][3]
Indicada quando a história sugere obstrução do trato urinário [3]
Doppler intrarrenal: técnica emergente para avaliar congestão venosa renal e índice de resistência vascular [1]
É operador-dependente e com variabilidade interobservador considerável [1]
TC sem contraste: indicada para litíase renal ou ureteral [2]
Pielografia ou TC com contraste: para causas obstrutivas sem hidronefrose (fibrose retroperitoneal, malignidade) [1]
Exames contrastados (incluindo RM com gadolínio) devem ser evitados na LRA pelo risco de fibrose nefrogênica sistêmica [7]
RM multiparamétrica avançada: permite mensurações quantitativas simultâneas de morfologia, microestrutura, oxigenação, fluxo e perfusão renal; ainda restrita ao ambiente de pesquisa [1]
Biópsia Renal
Reservada para LRA intrínseca sem causa clara ou quando múltiplas etiologias são possíveis [2][3]
Indicada principalmente em: suspeita de GN rapidamente progressiva, NIA com necessidade de confirmação diagnóstica antes de corticoterapia, evolução atípica ou prolongada, necrose cortical, doença ateroembólica, vasculites [3][5][7]
A imunofluorescência, microscopia eletrônica e colorações para fibrose e células inflamatórias auxiliam na diferenciação etiológica [2]
Cautela em rim único ou coagulopatia [2]
Diagnóstico Diferencial
LRA Pré-renal vs. NTA
Os índices urinários auxiliam no diagnóstico diferencial das oligúrias. [7]
A FENa apresenta o melhor desempenho entre os índices tradicionais, mas é falseada por diversas situações prevalentes em pacientes com LRA: ausência de oligúria, disfunção hepática, uso de diuréticos de alça, manitol, contraste radiológico ou excreção de elevada carga osmolar por aporte dietético.
Nesses casos, a FEU é preferível. Nenhum dos índices oferece discriminação perfeita e devem ser utilizados como ferramentas auxiliares.
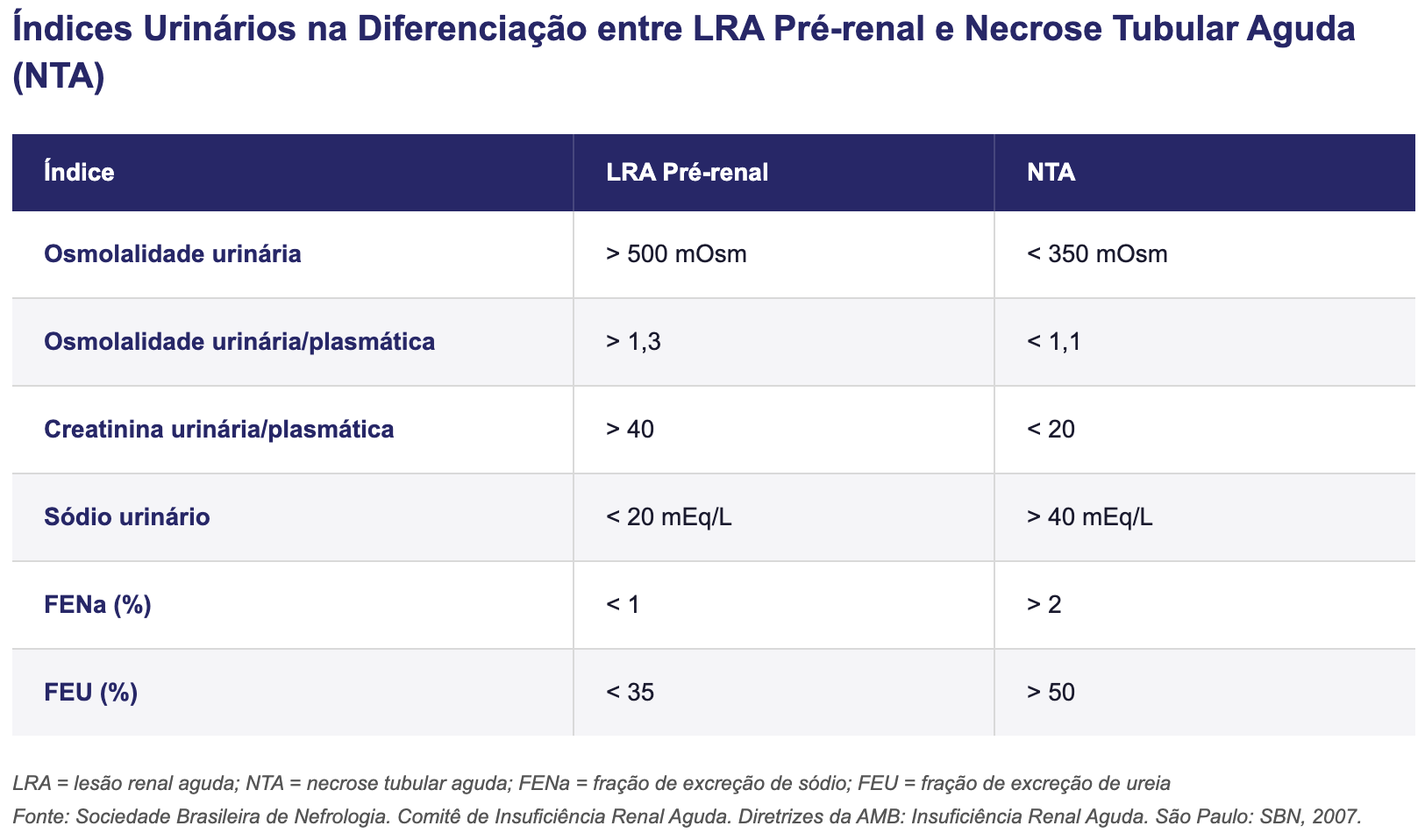
FEU: [(ureia urinária / ureia plasmática) / (creatinina urinária / creatinina plasmática)] × 100 (%)
Em pacientes oligúricos com FENa ou FEU elevadas, ressuscitação volêmica forçada não tem capacidade de melhorar a função renal e pode resultar em edema pulmonar, hipóxia, necessidade de ventilação mecânica e SDRA [7]
LRA vs. DRC
Sugestivos de DRC: perda de função renal lenta e progressiva, presença de sinais e sintomas de uremia avançada (anemia, coloração amarelo-palha, sintomas neurológicos e digestivos), cilindros largos no sedimento urinário [7]
Antecedentes de HAS, diabetes, nefropatias e doença vascular podem auxiliar, mas também são causas predisponentes para LRA agudizada (LRA que se desenvolve em pacientes com comprometimento prévio da função renal) [7]
Ultrassonografia: rins contraídos ou hipercogênicos sugerem DRC; rins de aspecto normal ou aumentado sugerem LRA
Exceção: nefropatia diabética pode evoluir para DRC com aspecto sonográfico renal próximo da normalidade [7]
Fatores de Risco e Prevenção
Fatores de Risco Não modificáveis: [3][6]
DRC prévia (fator de risco mais forte; reduz reserva funcional renal) [6]
AIDS, hepatopatia crônica, ICC, DM
Doença vascular periférica, estenose de artéria renal
Idade ≥ 65 anos, sexo masculino (em modelos pré-clínicos; evidências clínicas mistas) [1]
Fatores de Risco Modificáveis: [3]
Anemia, hipocolesterolemia, hipertensão, hipoalbuminemia, hiponatremia
Ventilação mecânica, sepse
Uso de medicamentos nefrotóxicos
Rabdomiólise
Contexto específico de UTI cardíaca: [6]
Maior tamanho do infarto e Killip mais alto em SCA
Uso de contraste iodado em intervenções coronarianas percutâneas (LRA por contraste em aproximadamente 15% dos casos)
Prevenção ↓
Princípios gerais: [1][7]
Estabelecer nível basal de função renal por dosagem de creatinina sérica ou clearance estimado antes de procedimentos ou exposições de risco [7]
Otimizar condições clínicas: expandir volume intravascular adequadamente; manter PAM > 80 mmHg (ou mais em hipertensos), hematócrito > 30% e oxigenação tecidual adequada [7]
Em pacientes sob terapia intensiva com vasoativos: utilizar medidas complementares para avaliação da volemia (PVC, SvO₂, ecocardiografia, variação da pressão de pulso/deltaPP) [7]
Evitar drogas nefrotóxicas em pacientes com função renal comprometida; ajustar doses conforme a função renal; manter hidratação adequada; evitar associação de nefrotoxinas [7]
Não utilizar diuréticos de alça para prevenção de nefrotoxicidade [7]
Em mioglobinúria e hemoglobinúria: expansão com solução salina isotônica é a estratégia principal com evidência mais robusta (KDIGO 2012, Grau 1A); o uso adicional de bicarbonato de sódio e manitol é suportado por dados observacionais e recomendado pela SBN 2007 [7], mas não há ensaios clínicos randomizados que comprovem benefício adicional sobre a salina isolada
Tratamento dos fatores precipitantes e prevenção de novas agressões nefrotóxicas [1]
Bundles de cuidado guiados por biomarcadores (IGFBP7 × TIMP-2) reduzem desenvolvimento de LRA moderada a grave após cirurgia cardíaca e não cardíaca (ensaios PrevAKI, BigpAK) [1][8]
Sistemas de suporte à decisão clínica associados a redução de 2,3% na incidência de LRA por contraste (estudo em coorte com intervenção escalonada) [1]
Período perioperatório: [1]
Evitar hipovolemia e hipotensão antes e durante cirurgias
Manutenção da pressão arterial sistólica próxima ao basal intraoperatório associa-se a menor risco de LRA pós-operatória
IECA/BRA podem ser mantidos perioperatoriamente na ausência de hipotensão intraoperatória grave (ensaio Stop-or-Not, n = 2.222)
Bypass cardiopulmonar sem circulação extracorpórea (off-pump) associa-se a menor incidência de LRA pós-operatória
Infusão IV perioperatória de aminoácidos reduziu risco de LRA em ECR multicêntrico publicado em 2024 [1]
LRA Associada ao Contraste Iodado (CA-AKI e CI-AKI): [9]
O ACR e a NKF estabeleceram terminologia harmonizada para as formas de LRA relacionadas ao contraste:
CA-AKI (contrast-associated acute kidney injury): deterioração súbita da função renal que ocorre dentro de 48h após a administração intravascular de contraste iodado, independentemente de causalidade; é um diagnóstico correlativo
CI-AKI (contrast-induced acute kidney injury): deterioração renal causada diretamente pelo contraste iodado; é um diagnóstico causativo e subgrupo da CA-AKI
Muito poucos estudos publicados dispõem de grupo controle adequado para separar CI-AKI de CA-AKI; a incidência relatada de CA-AKI inclui uma combinação de CI-AKI e LRA coincidente não causada pelo contraste
Patogênese: [9]
Fatores etiológicos sugeridos para a CI-AKI: alterações hemodinâmicas renais (vasoconstrição) e toxicidade tubular direta
A dose de contraste por via intra-arterial suprarrenal (cateterismo cardíaco) resulta em exposição renal mais abrupta e concentrada do que a via IV; estudos de cateterismo cardíaco superestimam o risco de CI-AKI para pacientes submetidos a contraste IV
Meios de contraste à base de gadolínio não causam CI-AKI em doses aprovadas pelo FDA
Diagnóstico de CA-AKI/CI-AKI: [9]
Critérios KDIGO são recomendados pelo ACR e pela NKF para diagnóstico:
Aumento absoluto de creatinina ≥ 0,3 mg/dL
Aumento percentual da creatinina ≥ 50% (≥ 1,5× o basal)
Débito urinário ≤ 0,5 mL/kg/h por pelo menos 6h
Curso clínico habitual: creatinina começa a elevar-se em 24h, atinge pico em 4 dias e retorna ao basal em 7–10 dias; disfunção renal permanente é incomum
Fatores de risco e limiares de eGFR: [9]
Principal fator de risco: insuficiência renal pré-existente grave (eGFR < 30 mL/min/1,73 m²)
Em pacientes com eGFR estável ≥ 45 mL/min/1,73 m², contraste IV não é fator de risco nefrotóxico independente
Em pacientes com eGFR estável 30–44 mL/min/1,73 m², contraste IV raramente é nefrotóxico
Limiar de 30 mL/min/1,73 m² é o com maior nível de evidência para estratificação de risco de CI-AKI
Pacientes com DRC terminal anúrica (sem rim transplantado funcionante) não estão em risco de CI-AKI e podem receber contraste iodado intravascular sem risco adicional de lesão renal
Indicações para avaliação da função renal antes do contraste iodado: [9]
História pessoal de doença renal: DRC conhecida, LRA prévia, diálise, cirurgia ou ablação renal, albuminúria
Uso de metformina ou formulações combinadas contendo metformina (pelo risco de acidose lática se CI-AKI ocorrer)
Diabetes mellitus (opcional)
Pacientes sem esses fatores de risco não requerem dosagem de creatinina/eGFR de rotina antes do contraste
Intervalo máximo aceito entre avaliação renal e administração do contraste: 30 dias em pacientes ambulatoriais; intervalo menor é prudente em pacientes internados ou com novo fator de risco
Prevenção de CI-AKI: [9]
A principal ação preventiva é a expansão volêmica intravascular:
Expansão volêmica com soro fisiológico (SF) 0,9%:
Fluido de escolha; SF 0,9% é superior ao SF 0,45% em reduzir o risco de CA-AKI
Regimes típicos: iniciar 1h antes do exame e manter por 3–12h após (regimes de ~12h demonstraram maior benefício)
Doses: volume fixo (ex.: 500 mL de SF) antes e após, ou volumes peso-ponderados (1–3 mL/kg/h)
Indicado para: pacientes com LRA ativa ou DRC grave (eGFR < 30 mL/min/1,73 m²), considerando contraindicações como ICC
Não indicado de rotina para: população geral com eGFR estável ≥ 30 mL/min/1,73 m² ou pacientes em diálise crônica
Pode ser considerado individualmente para pacientes com eGFR 30–44 mL/min/1,73 m² em circunstâncias de alto risco
Bicarbonato de sódio IV:
Provavelmente similar ao SF 0,9% para prevenção de CA-AKI; não preferido por exigir manipulação farmacêutica adicional
N-acetilcisteína (NAC):
Ensaio clínico randomizado demonstrou que a NAC não é superior ao placebo na prevenção de CA-AKI para contraste intra-arterial; não é recomendada para profilaxia
Manitol e furosemida:
Manitol não demonstrou benefício quando adicionado à solução salina IV
Furosemida agravou a disfunção renal quando utilizada em adição ao SF IV
Nenhum dos dois é recomendado para redução do risco de CI-AKI
Outros agentes (teofilina, endotelina-1, fenoldopam):
Não recomendados; evidências insuficientes
Escolha do meio de contraste: [9]
Meios de contraste de baixa osmolaridade (LOCM) são menos nefrotóxicos do que os de alta osmolaridade (HOCM) em pacientes com insuficiência renal prévia; HOCM não é mais utilizado para fins intravasculares na maioria dos centros
Não há vantagem clara do iodixanol (iso-osmolar) sobre os LOCM para CA-AKI ou CI-AKI por via IV
Pacientes em diálise: [9]
Pacientes em hemodiálise que produzem > 1–2 copos de urina/dia (236–473 mL/dia) devem ser tratados como pacientes de alto risco (não anúricos)
Não se recomenda iniciar ou ajustar programação de diálise ou TRRC com base exclusiva na administração de contraste iodado, independentemente da função renal
Metformina e contraste iodado: [9]
A metformina não confere risco aumentado de CI-AKI; no entanto, se CI-AKI ocorrer em paciente em uso de metformina, pode haver acúmulo do fármaco com risco de acidose lática
Categoria I (eGFR ≥ 30 mL/min/1,73 m², sem LRA ativa): não é necessário suspender a metformina antes ou após o contraste IV, nem reavaliar obrigatoriamente a função renal após o exame
Categoria II (LRA ativa ou DRC grave: eGFR < 30 mL/min/1,73 m²; ou cateterismo arterial com risco de êmbolos renais): suspender a metformina no momento do procedimento e por 48h após; reintroduzir somente após reavaliação da função renal
Estatinas em alta dose e LRA por contraste: [3]
Meta-análise de 15 ECRs demonstrou redução de CA-AKI em pacientes submetidos a cateterismo cardíaco/ICP com estatinas em alta dose (atorvastatina, rosuvastatina, sinvastatina) vs. baixas doses ou placebo (ARR = 2,8%; NNT = 36)
Inibidores de SGLT2: [1]
Meta-análise de 13 ensaios demonstrou redução de 23% no risco de LRA com inibidores de SGLT2 vs. placebo (RR 0,77; IC 95% 0,70–0,84)
Descontinuação adequada em casos de choque, acidose metabólica ou ITU grave; manutenção deve ser considerada em pacientes com indicação forte (ex.: insuficiência cardíaca grave)
Manejo
Princípios Gerais
O manejo da LRA é primariamente de suporte, centrado no tratamento da causa subjacente, prevenção de novas lesões e controle das complicações. Exceções com terapias específicas incluem: imunossupressão para GN e NIA, terlipressina para SHR e alívio cirúrgico ou endoscópico da obstrução pós-renal. [1][3]
Manejo de Drogas
Suspender, reduzir ou evitar drogas diretamente nefrotóxicas [1][3]
Programas de stewardship nefrotóxico reduzem exposições e incidência de LRA em ambiente hospitalar [3]
IECA/BRA podem frequentemente ser mantidos na ausência de hipotensão ou hipercalemia, especialmente em SCR [1]
Drogas de eliminação renal que requerem ajuste de dose na LRA: [3]
Analgésicos: morfina, meperidina, gabapentina, pregabalina
Antiepilépticos: lamotrigina
Antivirais: aciclovir, ganciclovir, valganciclovir
Antifúngicos: fluconazol
Antimicrobianos: quase todos requerem ajuste (exceções: azitromicina, ceftriaxona, doxiciclina, linezolida, moxifloxacino, nafcilina, rifampicina)
Antidiabéticos: sulfonilureias, metformina
Outros: alopurinol, baclofeno, colchicina, digoxina, lítio, HBPM, NOACs
Manejo de Fluidos
Objetivo: atingir euvolemia sem causar ou agravar sobrecarga hídrica [1][3]
Tanto hipovolemia quanto hipervolemia determinam a progressão e a recuperação da LRA [1]
Cristaloides balanceados (Ringer lactato, Plasma-Lyte) são preferíveis ao soro fisiológico 0,9%, associando-se a menor mortalidade e menor necessidade de TRS em pacientes críticos e não críticos (exceto em TCE) [1][3]
Albumina: não reduz risco de LRA grave na sepse; recomendada em paracentese de grande volume, peritonite bacteriana espontânea e SHR com terlipressina [1]
Coloides sintéticos (amido hidroxietílico): aumentam risco de TRS e devem ser evitados [1]
Diuréticos de alça: indicados para tratar hipervolemia; não têm papel no tratamento da LRA oligúrica em si nem na conversão de LRA oligúrica para não oligúrica [1][2]
Manejo Hemodinâmico
Reversão rápida da hipotensão para pressão acima do limiar de autorregulação renal pode prevenir progressão da LRA [1]
Meta inicial de pressão arterial média: 65 mmHg para a maioria dos pacientes; individualizar conforme valores prévios e marcadores de perfusão [1]
Em pacientes hipertensos crônicos, alvos mais elevados de PAM podem ser benéficos para função renal (resultados inconsistentes entre os ensaios) [1]
Norepinefrina: vasopressor de primeira linha na LRA [1]
Fluidos para hipovolemia; vasopressores para vasoplegia; inotrópicos para disfunção cardíaca com baixo débito
Análise post-hoc do ensaio ATHOS-3: pacientes em TRS com choque vasodilatador randomizados para angiotensina II apresentaram melhor sobrevida e liberação mais precoce da TRS [1]
Suporte Nutricional
Ingestão calórica e proteica prescrita como para outros pacientes hospitalizados [1]
Entrega de proteína em alta quantidade pode aumentar mortalidade em pacientes críticos com LRA [1]
Restrições de potássio, fósforo e sódio se aplicam à maioria dos pacientes com LRA
Evitar hiperglicemia; meta glicêmica de 110–149 mg/dL para pacientes em UTI, conforme recomendação do KDIGO 2012 (Grau 2C) [3]; diretrizes gerais de terapia intensiva (SCCM/ASPEN 2016; ESICM/ESPEN 2019) recomendam alvo de 140–180 mg/dL para pacientes críticos em geral — o alvo mais estrito é defensável no contexto específico da LRA, mas deve ser individualizado
Suplementação de micronutrientes recomendada para pacientes recebendo TRS [1]
Evitar hiperhidratação, que pode causar edema, hipertensão, insuficiência cardíaca e hiponatremia; a LRA é processo hipercatabólico e paciente que não perder cerca de 300 g/dia de peso corporal quase certamente está em balanço hídrico positivo [7]
Complicações e Manejo
Hipercalemia: [2]
Potencial para arritmias; emergência médica quando grave (K > 6,5 mEq/L com alterações eletrocardiográficas)
Manejo: restrição dietética, insulina + dextrose IV, β-agonistas, resinas de troca catiônica, gluconato de cálcio para estabilização de membrana cardíaca, diálise para hipercalemia refratária
Acidose metabólica: [2]
Comum na LRA; raramente requer tratamento específico salvo se grave
Administração sistêmica de bicarbonato ou citrato quando indicado
Hiperfosfatemia:
Restrição dietética ou quelantes de fósforo [2]
Sobrecarga de fluidos:
Diuréticos de alça (altas doses IV) ou TRS [2]
Encefalopatia urêmica:
Sinais: letargia, sonolência, distúrbio do ciclo sono-vigília, comprometimento cognitivo [2]
Disfunção plaquetária:
LRA pode induzir disfunção plaquetária com risco aumentado de sangramento clinicamente significativo [1]
Manejo da SCR:
Terapia Diurética Escalonada
Para pacientes com IC aguda e SCR, diuréticos de alça são a primeira linha para remoção de volume. Diurese bem-sucedida pode melhorar a função renal ao aliviar a congestão venosa renal. [6]
Algoritmo escalonado de diuréticos (CARRESS-HF/AVOID-HF): [6]
Passo 1 (furosemida ≤ 80 mg/dia prévia): furosemida 40 mg IV + infusão de 5 mg/h
Passo 2 (81–160 mg/dia prévia): furosemida 80 mg IV + 10 mg/h + metolazona 5 mg 1×/dia
Passo 3 (161–240 mg/dia prévia): furosemida 80 mg IV + 20 mg/h + metolazona 5 mg 2×/dia
Passo 4 (> 240 mg/dia prévia): furosemida 80 mg IV + 30 mg/h + metolazona 5 mg 2×/dia
Considerações:
Meta de débito urinário: 3–5 L/dia; escalar dose se débito < 3 L/dia
Vasoativo ou inotrópico pode ser adicionado no passo 4 sem resposta adequada
Adição de segundo diurético (tiazídico em primeira linha; espironolactona ou tolvaptan em segunda linha) pode superar resistência diurética. [6]
Ultrafiltração isolada (aquaferese):
Alternativa para IC refratária com resistência diurética [6]
Preferível em pacientes com creatinina < 2,5 mg/dL; acima deste valor, modalidades de TRS com clearance de solutos são preferíveis
Não demonstrou superioridade à terapia diurética escalonada no ensaio CARRESS-HF
Parece mais benéfica quando iniciada nas primeiras 24h da admissão [6]
Manejo da SHR
Terlipressina em combinação com albumina 20–25%: agentes de primeira linha para reversão da SHR-LRA [1]
Janela de 24h para avaliação da resposta volêmica (quando indicada), evitando sobrecarga hídrica e garantindo início oportuno de vasoconstritores
Norepinefrina tem eficácia comparável à terlipressina conforme meta-análises [1]
Monitoramento rigoroso do estado volêmico durante terlipressina; ajuste ou interrupção em caso de sobrecarga ou ausência de resposta [1]
Terapia de Substituição Renal (TRS)
A TRS constitui um processo de cuidado contínuo que requer avaliação, monitoramento e reavaliação regulares. [1]
Objetivos da TRS na LRA [7]
Correção das anormalidades metabólicas decorrentes da disfunção renal
Regulação do equilíbrio ácido-básico, eletrolítico, hídrico, volêmico e nutricional
Manejo do líquido extracelular em falência orgânica múltipla
Preservação e auxílio na recuperação das disfunções orgânicas (renal, SNC, cardiovascular, respiratória, gastrointestinal)
Manipulação e remoção de mediadores que contribuem para a desregulação da resposta inflamatória na doença crítica (eventualmente)
Indicações de Diálise na LRA
A melhor conduta é prevenir a necessidade de diálise de urgência pela indicação precoce, antes do surgimento de uremia franca e/ou de complicações clínicas, metabólicas e eletrolíticas. [7]
Indicações urgentes/absolutas: [1][2][3][6][7]
Hipercalemia grave refratária ao tratamento medicamentoso: K > 5,5 mEq/L com alterações ao ECG ou K > 6,5 mEq/L [7]
Acidose metabólica grave refratária (pH < 7,2 com pCO₂ normal ou baixo)
Sobrecarga de fluidos com edema pulmonar não responsiva a diuréticos
Uremia sintomática: encefalopatia, neuropatia urêmica, pericardite e tamponamento pericárdico [7]
Azotemia grave: ureia N (BUN) > 84 mg/dL (> 30 mmol/L) — equivalente a ureia total > 180 mg/dL nos padrões laboratoriais brasileiros
Anúria por ≥ 6h ou oligúria < 200 mL em 12h
Intoxicação por drogas dialisáveis (etilenoglicol, lítio)
Outras: hipo ou hipernatremia, hipo ou hipercalcemia, hiperuricemia, hipermagnesemia, hemorragias por distúrbios plaquetários, ICC refratária, hipotermia [7]
Indicações específicas em UTI cardíaca (CICU): [6]
Disfunção cardíaca/valvar grave com PA limítrofe, LRA e sobrecarga volêmica
Choque cardiogênico ou IC com edema pulmonar em ventilação mecânica com FiO₂ > 80–90% apesar de diurético
Remoção de volume pré-cirúrgica cardíaca para facilitar fechamento do tórax
SCR refratária com LRA progressiva (estágio 2 a 3) e sobrecarga sem resposta diurética
Timing
Na ausência de indicações urgentes, ensaios clínicos (AKIKI, IDEAL-ICU, STARRT-AKI, 2016–2020) suportam estratégia de watchful waiting [1][6]
Iniciação de TRS sem indicação urgente não melhora desfechos clínicos; deferimento reduz utilização de TRS em aproximadamente 40% [1]
Exceção: ensaio ELAIN demonstrou melhor sobrevida com TRS precoce no estágio 2 em população cirúrgica com NGAL > 150 ng/mL [1][6]
Ensaio AKIKI-2: deferimento excessivo em LRA estágio 3 com oligúria > 72h e ureia > 140 mg/dL associou-se a maior mortalidade em 60 dias [1]
Pacientes sem indicação urgente podem ser observados com segurança inicial, inclusive na presença de oligúria (débito < 400–500 mL/dia); sobrecarga hídrica sintomática refratária a diuréticos deve motivar consideração de TRS [6]
Modalidades ↓
Métodos intermitentes: [1][6][7]
TRS intermitente convencional (HDI): 3–6h/dia
Hemodiálise prolongada (SLED/HDP): duração intermediária
Hemofiltração intermitente
Diálise peritoneal intermitente
Métodos contínuos (TRRC): [1][6][7]
Ultrafiltração contínua lenta (SCUF)
Hemofiltração veno-venosa contínua (CVVH)
Hemodiálise veno-venosa contínua (CVVHD)
Hemodiafiltração veno-venosa contínua (CVVHDF)
Diálise peritoneal ambulatorial contínua
Comparação TRRC vs. HDI: [1][6]
Ensaios clínicos não demonstraram diferença de sobrevida entre as modalidades
Análise secundária do STARRT-AKI: TRRC como modalidade inicial associou-se a menor risco de morte ou dependência dialítica em 90 dias [1]
TRRC é preferencial em lesão cerebral aguda/hipertensão intracraniana e instabilidade hemodinâmica
HDI é preferível para correção rápida de distúrbios hidroeletrolíticos graves, intoxicações e edema pulmonar agudo
Modalidades intermitentes oferecem maior mobilidade e menor custo
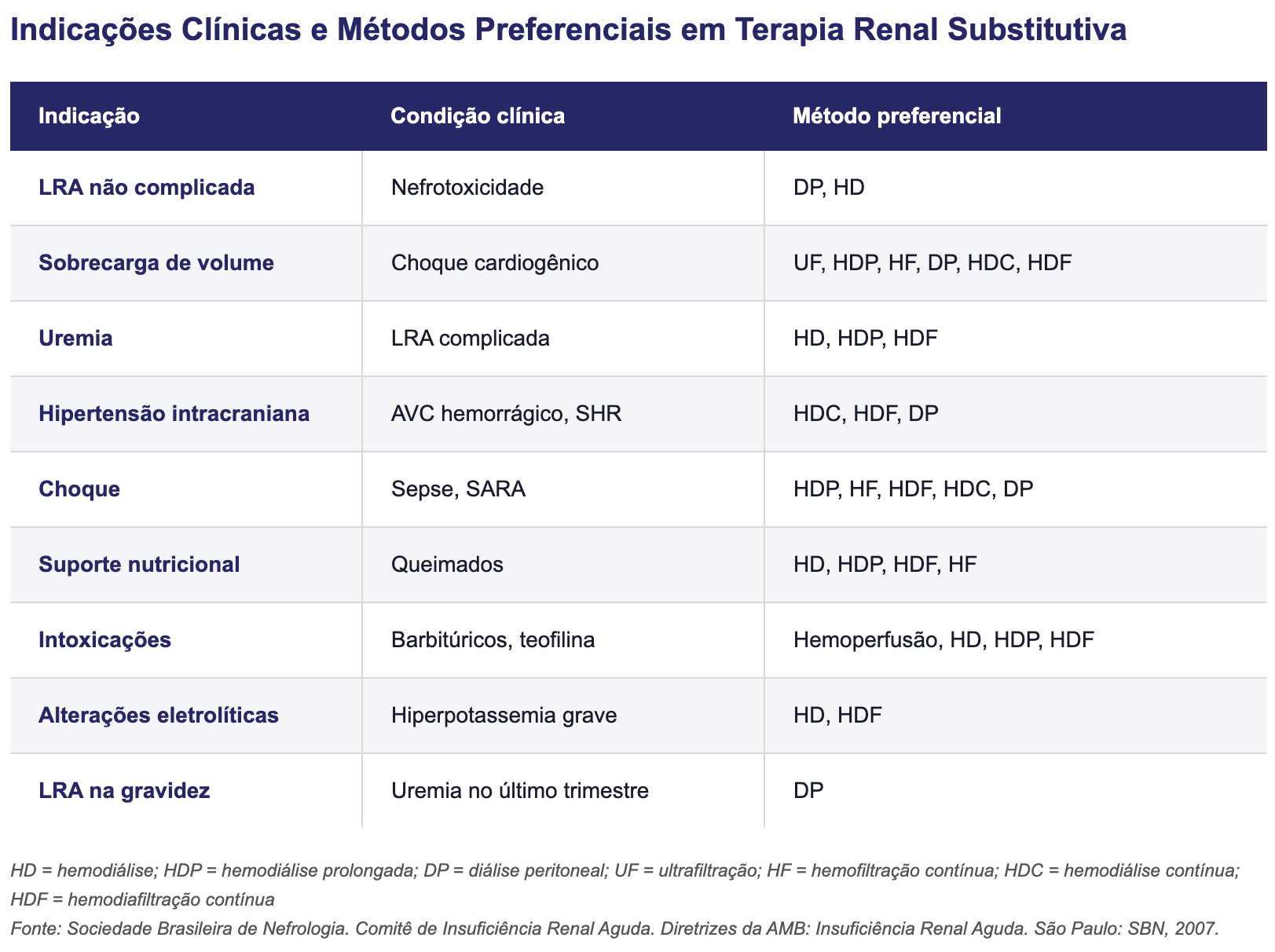
A escolha depende do julgamento clínico do nefrologista considerando a complexidade e instabilidade do quadro; não se deve retardar o início da diálise. [7]
Dose:
TRRC: recomenda-se prescrever dose de 25–30 mL/kg/h (dose de efluente total); doses mais altas não melhoram desfechos [1]
HDI: Kt/V de ureia semanal de 3,9 [1]
Taxa de ultrafiltração segura: 1,01–1,75 mL/kg/h; taxas > 1,75 mL/kg/h associam-se a piores desfechos [1][6]
Anticoagulação
A anticoagulação é obrigatória nos métodos hemodialíticos, interferindo diretamente na eficiência e durabilidade da terapêutica dialítica. A heparina é o agente mais utilizado. A escolha deve ser individualizada para cada paciente e relacionada ao caso clínico. [7]
Critérios de alto risco para anticoagulação: [7]
Critérios:
Contagem de plaquetas < 60.000/mL
TTPa > 60 segundos
INR > 2
Coagulação intravascular disseminada (CIVD)
Insuficiência hepática grave
Pós-operatório imediato
Nesses grupos, procedimentos sem anticoagulação ou com esquemas regionais oferecem menor risco de complicações hemorrágicas. [7]
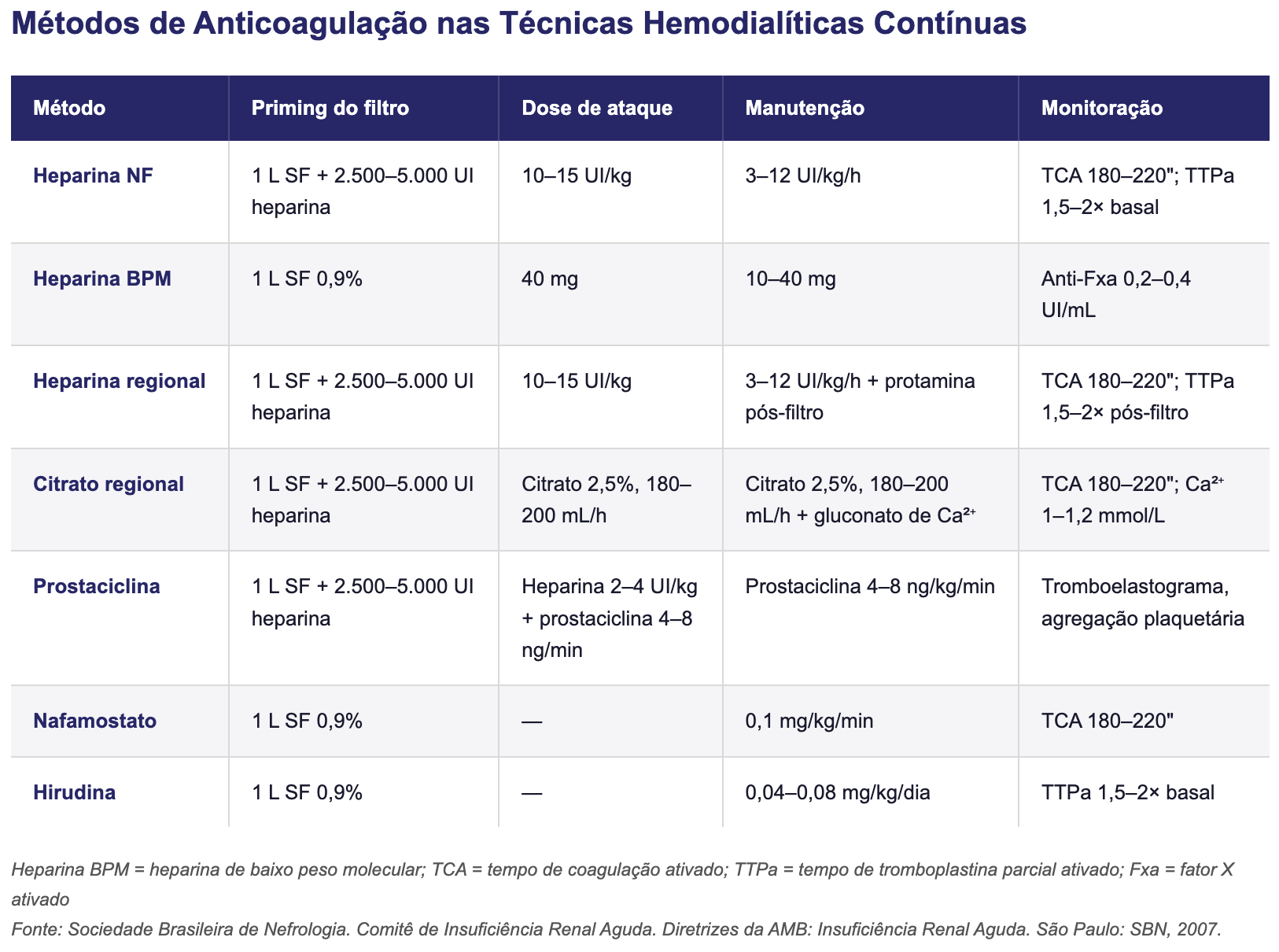
Sobre o citrato regional: [1][6]
Crescente uso na TRRC; melhor perviedade de filtro e menos complicações hemorrágicas vs. heparina
Requer monitoramento rigoroso de cálcio ionizado (6–12h) e acesso venoso central adicional para reposição de cálcio sistêmico
Acúmulo de citrato: acidose metabólica com ânion-gap elevado + hipocalcemia ionizada; razão cálcio total/ionizado > 2,4 sugere acúmulo e associa-se a maior risco de morte [6]
Contraindicação relativa em insuficiência hepática grave ou choque profundo [6]
Descontinuação da TRS
Creatinina e toxinas urêmicas são removidas pela TRS e não são indicadores confiáveis de recuperação renal [1]
Critérios amplamente aceitos para considerar descontinuação: [1][6]
Débito urinário espontâneo > 500 mL/dia sem diuréticos
Débito urinário > 2,4 L/dia com uso de diuréticos
Para TRRC: débito urinário ≥ 400 mL em 24h sem diuréticos (VPP 80,9%; VPN 76,5%) [6]
FST prediz descontinuação de TRS com AUROC = 0,84; evidências insuficientes para uso rotineiro de biomarcadores individuais para guiar a descontinuação [8]
Cistatina C mais elevada ao momento da descontinuação associa-se independentemente à dependência crônica de diálise [8]
Uso de diuréticos após descontinuação pode aumentar volume urinário, sem diferença em recuperação renal ou necessidade de novo ciclo de TRS [1][6]
Dosagem de Drogas na TRS
Ajuste de dose é particularmente desafiador durante TRS, especialmente em transições de modalidade e recuperação da função renal [1][6]
Tanto subdosagem quanto superdosagem de antimicrobianos foram relatadas [1]
Monitoramento farmacocinético terapêutico e modelos avançados de farmacocinética são estratégias emergentes [1]
Milrinona acumula durante LRA (meia-vida de até 20h em CVVH); deve ser usado com cautela ou evitado [6]
Antiarrítmicos de excreção renal podem acumular a níveis tóxicos em LRA grave [6]
Desfechos e Seguimento Pós-LRA
Recuperação Renal
Recuperação completa: retorno da creatinina ao valor basal [1]
Recuperação parcial: resolução da LRA sem retorno ao basal [1]
Reversão rápida: resolução em ≤ 48h; tardia: persistência > 48h [1]
Observações:
Em coorte de 16.968 pacientes críticos com LRA estágio 2 ou 3: [1]
41% não haviam recuperado completamente a função renal na alta hospitalar
26% sem reversão em nenhum momento; 15% com reversão seguida de recaída
Recuperação após 10 dias associa-se a maior risco de queda sustentada de TFGe ou falência renal. Pacientes com LRA não resolutiva têm risco 51% maior de eventos renais adversos maiores vs. aqueles com LRA resolutiva. [1]
LRA recorrente:
25% dos pacientes hospitalizados com LRA experimentam recorrência nos 12 meses após a alta (mediana de 64 dias); associada a maior risco de morte. [1]
Desfechos de Longo Prazo
DRC: risco aumenta de forma graduada com maior estágio KDIGO; LRA sobre DRC prévia eleva o risco de DRET em até 40 vezes [3]
MAKE em 1 ano: 37% dos pacientes hospitalizados com LRA; em pacientes críticos com LRA, 94% experimentaram MAKE em 3 anos [1]
Proteinúria pós-LRA: para cada duplicação da uACR, o HR para progressão renal foi 1,53 (IC 95% 1,45–1,62) no estudo ASSESS-AKI [1]
Comorbidades cardiovasculares: risco aumentado de MACE, insuficiência cardíaca, eventos coronarianos, hipertensão, AVC [1][3]
Outras complicações: infecção grave, hemorragia gastrointestinal superior, fraturas, demência, malignidade [1]
Mortalidade: [1][2][7]
Hospitalar: 24% em adultos e 14% em crianças; > 50% em pacientes de UTI
Mortalidade hospitalar da LRA: aproximadamente 50% apesar dos avanços tecnológicos [7]
Em UTI cardíaca com TRRC: mortalidade hospitalar ≥ 40–50%; mortalidade em 1 ano > 70% [6]
Causas mais frequentes de morte após LRA: doença cardiovascular e câncer [1]
Fatores preditores de pior prognóstico: oligúria, falência de múltiplos órgãos e septicemia [1][2][7]
Há evidências recentes de queda da mortalidade nos últimos anos [7]
Qualidade de vida:
Estudos relatam QV relacionada à saúde reduzida após LRA grave e doença crítica [1]
Fragilidade é comum em sobreviventes de LRA, especialmente nos casos mais graves [1]
Em crianças sobreviventes: déficits de memória e aprendizado foram relatados [1]
Taxas de morbidade e mortalidade mais elevadas a longo prazo em sobreviventes de LRA; necessidade de seguimento ambulatorial após a alta hospitalar [7]
Seguimento Pós-Alta
KDIGO recomenda avaliação 3 meses após LRA para resolução, novo surgimento ou piora de DRC prévia [1][3]
Se recuperação ≥ 90% do basal: seguimento em 3 meses; se recuperação mais lenta: seguimento em 3 semanas e novamente em 3 meses [3]
Monitorar em cada visita: PA, peso corporal, creatinina sérica e TFGe estimada [3]
Consulta com nefrologia se TFGe persistir < 60 mL/min/1,73 m² [3]
Biomarcadores preditivos de progressão para DRC (declaração 11 do consenso ADQI) devem ser incorporados ao cuidado pós-alta, direcionando recursos para os pacientes com maior probabilidade de benefício [1][8]
Biomarcadores mensurados 3 meses após LRA: TNFR1 e TNFR2 plasmáticos elevados no dia 1 associam-se à recuperação renal mais lenta e à mortalidade em pacientes com LRA em TRS [1][8]
Critérios para Encaminhamento à Nefrologia
Consulta nefrológica precoce (≤ 48h) está associada a melhores processos de cuidado e desfechos. [3]
Indica-se quando: [3][6]
LRA estágio 3 ou superior
LRA sem causa clara
DRC prévia estágio 4 ou superior
Necessidade de TRS
Suspeita de GN ou vasculite (encaminhar com urgência)
Resposta inadequada ao tratamento de suporte
Situações que requerem expertise subespecializada: transplante renal, mieloma múltiplo, GN, síndrome nefrótica
Referências
[1] OSTERMANN, M.; LUMLERTGUL, N.; JEONG, R. et al. Acute kidney injury. Lancet, v. 405, p. 241–256, 18 jan. 2025. Disponível em: https://doi.org/10.1016/S0140-6736(24)02385-7. Acesso em: 27 abr. 2026.
[2] GOYAL, A.; DANESHPAJOUHNEJAD, P.; HASHMI, M.F.; BASHIR, K. Acute Kidney Injury. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2026. Disponível em: https://www.ncbi.nlm.nih.gov/books/NBK441896/. Acesso em: 27 abr. 2026.
[3] MERCADO, M.G.; SMITH, D.K.; GUARD, E.L. Acute Kidney Injury: Diagnosis and Management. American Family Physician, v. 100, n. 11, p. 687–694, dez. 2019. Disponível em: https://www.aafp.org/afp/2019/1201/p687.html. Acesso em: 27 abr. 2026.
[4] TURGUT, F.; AWAD, A.S.; ABDEL-RAHMAN, E.M. Acute Kidney Injury: Medical Causes and Pathogenesis. Journal of Clinical Medicine, v. 12, n. 1, p. 375, 3 jan. 2023. Disponível em: https://doi.org/10.3390/jcm12010375. Acesso em: 27 abr. 2026.
[5] LIU, K.D.; KOYNER, J.L. Overview/Definition, Classification, and Epidemiology of Acute Kidney Disease. In: CRAIG, J.C.; MOLONY, D.A.; STRIPPOLI, G.F.M. (ed.). Evidence-Based Nephrology. 2. ed. Hoboken: John Wiley & Sons, 2023. cap. 7, p. 87–95. Disponível em: https://doi.org/10.1002/9781119105954.ch7. Acesso em: 27 abr. 2026.
[6] JENTZER, J.C.; BIHORAC, A.; BRUSCA, S.B. et al. Contemporary Management of Severe Acute Kidney Injury and Refractory Cardiorenal Syndrome: JACC Council Perspectives. Journal of the American College of Cardiology, v. 76, n. 9, p. 1084–1101, 1 set. 2020. Disponível em: https://doi.org/10.1016/j.jacc.2020.06.070. Acesso em: 27 abr. 2026.
[7] BRASIL. Sociedade Brasileira de Nefrologia. Comitê de Insuficiência Renal Aguda. Diretrizes da AMB: Insuficiência Renal Aguda. São Paulo: SBN, 2007. Disponível em: https://www.sbn.org.br. Acesso em: 27 abr. 2026.
[8] OSTERMANN, M.; ZARBOCK, A.; GOLDSTEIN, S. et al. Recommendations on Acute Kidney Injury Biomarkers From the Acute Disease Quality Initiative Consensus Conference: a Consensus Statement. JAMA Network Open, v. 3, n. 10, e2019209, 6 out. 2020. Disponível em: https://doi.org/10.1001/jamanetworkopen.2020.19209. Acesso em: 27 abr. 2026.
[9] AMERICAN COLLEGE OF RADIOLOGY. Committee on Drugs and Contrast Media. ACR Manual on Contrast Media. 2026. Disponível em: https://www.acr.org/Clinical-Resources/Contrast-Manual. Acesso em: 27 abr. 2026.
Autoria e Curadoria
As informações contidas nesta página são de autoria da Equipe Editorial Médica do GPMED, composta por médicos especialistas de diversas áreas. Todo o conteúdo é estruturado rigorosamente com base em fontes bibliográficas de alto impacto e nas diretrizes oficiais vigentes, seguindo os preceitos da Medicina Baseada em Evidências. Nosso compromisso é oferecer ao médico uma base de consulta técnica, confiável e chancelada por profissionais experientes, garantindo máxima segurança no suporte à decisão clínica.


