Nódulo Tireoidiano no Adulto
CID-10: E04.1 – Nódulo tireoidiano solitário não tóxico
CID-10: E04.2 – Bócio multinodular atóxico
Introdução
Nódulos tireoidianos representam a principal manifestação clínica de uma série de doenças da tireoide e constituem achado frequente na prática médica. [3][4]
Epidemiologia:
Estudos epidemiológicos em áreas suficientes em iodo demonstram que 4% a 7% das mulheres e 1% dos homens adultos apresentam nódulo palpável; quando avaliados por ultrassonografia (US), a prevalência é ainda maior, variando de 19% a 68%, com maior incidência em mulheres e idosos. [3][4][5]
Nódulos tireoidianos são aproximadamente quatro vezes mais comuns em mulheres do que em homens, e sua prevalência aumenta com a idade e o índice de massa corporal. [5]
Dados de autópsia demonstram prevalência de 50% de nódulos maiores que 1 cm em pacientes sem diagnóstico prévio de doença tireoidiana. [2]
Definição:
A Associação Americana da Tireoide (ATA) define nódulo tireoidiano como uma lesão discreta dentro da glândula, radiologicamente distinta do parênquima circundante; os nódulos podem ser solitários, múltiplos, císticos ou sólidos. [2]
Os casos mais frequentes são: cistos colóides e tireoidites (80%); neoplasias benignas (10–15%); e carcinomas (5–10%). [1]
Na maioria das vezes, apresentam evolução insidiosa e são descobertos incidentalmente em exames de imagem realizados por outros motivos, os chamados incidentalomas. [1]
Importância clínica:
A principal importância clínica no manejo dos nódulos baseia-se na necessidade de excluir malignidade, que ocorre em 5% a 10% dos casos; o risco de câncer é semelhante em nódulos palpáveis e incidentalomas, independentemente do tamanho. [3][4]
Os carcinomas diferenciados (papilífero e folicular) respondem por cerca de 90% das neoplasias malignas da tireoide. [4]
Os nódulos tireoidianos são mais comuns em idosos, mulheres, em locais com deficiência de iodo e em pacientes com história de exposição prévia à radiação. [1]
Fluxograma de Manejo
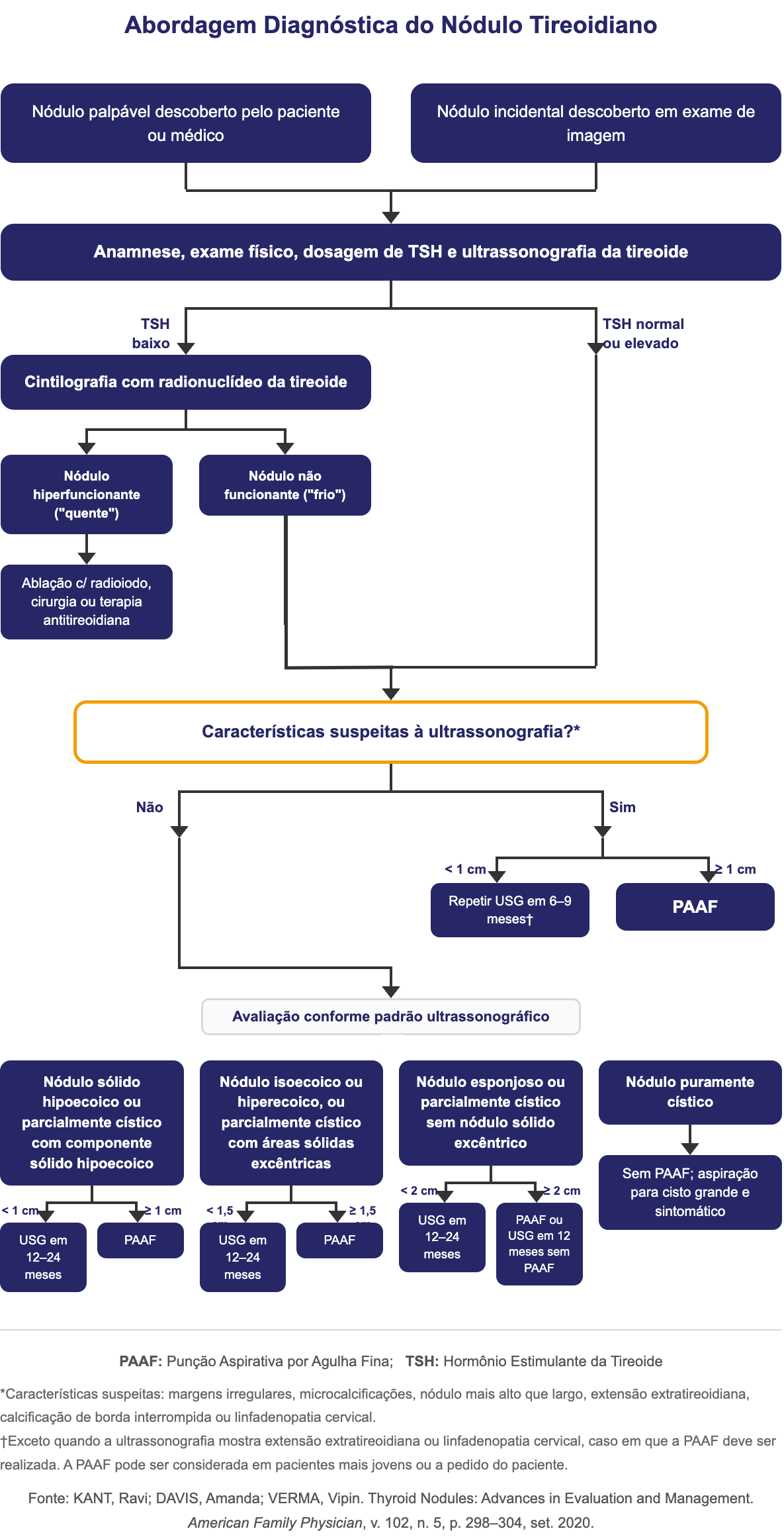
Fatores de Risco para Malignidade
A presença de fatores de risco deve orientar a investigação precoce, inclusive com indicação antecipada de PAAF, independentemente do tamanho do nódulo. [1]
Fatores epidemiológicos e de história clínica [1][3][4][5]
Sexo masculino
Idade < 20 anos ou > 60–70 anos
Radiação cervical prévia (terapêutica ou acidental; exposição pediátrica confere risco aumentado pela maior atividade proliferativa do tecido tireoidiano) [2]
História familiar de câncer de tireoide (principalmente papilífero e medular) ou síndromes endocrinológicas associadas (NEM2, Cowden, Pendred, Werner, Polipose adenomatosa familiar) [1]
Áreas com deficiência de iodo [1]
Sobreviventes de transplante de células-tronco hematopoiéticas (risco relativo de carcinoma secundário: 3,26) [2]
Sinais e sintomas de alarme [1][3][4]
Paralisia de cordas vocais / disfonia
Disfagia
Dispneia
Crescimento rápido do nódulo
Consistência endurecida ou fixação a planos profundos
Tamanho > 4 cm
Linfadenopatia cervical ipsilateral
Metástase à distância
Achados ultrassonográficos suspeitos [3][4][5]
Hipoecogenicidade intranodular
Microcalcificações
Margens irregulares ou espiculadas
Formato mais alto do que largo (em corte transversal)
Fluxo vascular predominantemente intranodular ao Doppler
Linfonodos cervicais anormais (> 7 mm no menor eixo, forma irregular, perda da hiperecogenicidade central, ecotextura heterogênea, calcificações internas, áreas de cistificação ou hipervascularização; excluindo-se os submandibulares) [3]
⚠️ Importante: A combinação de nódulo solitário + linfadenopatia cervical (> 1 cm) + paralisia de corda vocal tem valor preditivo positivo de aproximadamente 100% para malignidade tireoidiana. [2]
Avaliação Inicial
Diante da detecção de um nódulo tireoidiano, histórico clínico completo e exame físico cuidadoso devem ser realizados, visando à caracterização do nódulo e à avaliação de linfadenopatia cervical. [3][4]
Todo nódulo de tireoide deve ser investigado com métodos complementares; sejam incidentalomas ou nódulos palpáveis, independentemente do tamanho, o risco de câncer é semelhante [3]
Nódulos > 1 cm: avaliar sempre [4]
Nódulos ≤ 1 cm: avaliar se apresentarem características ultrassonográficas suspeitas ou história clínica de risco [4][5]
Avaliação Laboratorial
TSH sérico: exame inicial obrigatório em toda doença nodular tireoidiana [1][3][4][5]
TSH normal ou elevado: associado a maior risco de malignidade [3][4]
Se TSH elevado: solicitar anti-TPO para confirmar tireoidite de Hashimoto [3][4]
Na presença de Hashimoto com nódulo bem definido ao US: indicar PAAF para afastar carcinoma diferenciado ou linfoma (raro, mas frequentemente associado a tireoidites) [4]
TSH suprimido: avaliar nódulo hiperfuncionante por cintilografia tireoidiana (tecnécio-99 ou iodo-123) [3][4][5]
Se confirmado hiperfuncionante (quente): PAAF contraindicada; nódulos hiperfuncionantes raramente são malignos [1][4][5]
Se TSH suprimido confirmado: solicitar T4 livre e T3 livre para caracterizar hipertireoidismo [3]
Exames não recomendados na avaliação inicial [1][3][4]
Tireoglobulina (Tg): teste insensível para o diagnóstico de malignidade; não solicitar de rotina [3][4]
Calcitonina: não solicitar de rotina; indicada apenas na suspeita clínica de carcinoma medular (história pessoal ou familiar de NEM2 ou tumor medular) [1][3][4]
Avaliação por Imagem
Ultrassonografia (US)
A ultrassonografia convencional (com ou sem Doppler) é o principal método de imagem para avaliação dos nódulos tireoidianos e amplia em cinco vezes a detecção de nódulos não identificados à palpação. [3] Permite avaliar tamanho, ecogenicidade, bordos, calcificações, fluxo vascular e relação com estruturas cervicais, além de guiar a PAAF. [3][4]
Indicações do US cervical [3][5]
Suspeita clínica de doença nodular tireoidiana
Nódulo detectado por outro método de imagem (cintilografia, TC, RM)
Incidentaloma: todo nódulo detectado incidentalmente deve ter diagnóstico complementado por avaliação ultrassonográfica
Não deve ser utilizado como método de rastreamento em pacientes assintomáticos sem suspeita clínica [3]
Achados que aumentam o risco de malignidade ao US [2][3][4][5]
Hipoecogenicidade (especialmente muito hipoecóico, mais que a musculatura adjacente)
Microcalcificações
Margens lobuladas, irregulares ou espiculadas
Extensão extratireoidiana (invasão óbvia)
Formato mais alto do que largo (avaliado em imagem transversal)
Fluxo vascular predominante intranodular ao Doppler
Linfonodos cervicais anormais
Observações técnicas importantes [3]
O tamanho do nódulo per se (> ou < 1 cm) não define benignidade ou malignidade
O Doppler auxilia na estratificação do risco, mas não substitui a PAAF
O exame deve englobar todo o pescoço, incluindo compartimento visceral e linfático
A PAAF guiada por US aumenta a sensibilidade do método de 91,8% para 97,1% [3]
Cintilografia tireoidiana
Indicação principal: TSH subnormal (suspeita de nódulo hiperfuncionante) [4][5]
Nódulo quente (hipercaptante): quase sempre benigno; PAAF contraindicada [1][4]
Nódulo frio ou morno (hipocaptante): representa 90% dos nódulos; risco de malignidade de 14% a 22% [3][4][5]
Radioisótopos: pode ser realizada com iodo radioativo (¹³¹I ou ¹²³I) ou pertecnetato de Tecnécio (⁹⁹ᵐTc); radioisótopos iodados são preferidos, pois 3% a 8% dos nódulos que parecem funcionantes ao ⁹⁹ᵐTc não o são quando mapeados com iodo radioativo [3][4]
Limitações: não tem valor diagnóstico para distinguir malignidade de benignidade no nódulo frio [3][4]
Contraindicada na gestação [4]
TC, RM e PET-scan
TC e RM: raramente indicadas na avaliação do nódulo tireoidiano; não permitem diferenciar lesões benignas de malignas; úteis na avaliação de bócios mergulhantes e compressão traqueal [4]
PET-FDG: sensibilidade em torno de 60% para malignidade; não há evidências de superioridade diagnóstica para o nódulo tireoidiano; não substitui a PAAF [3][4]
Classificação ACR TI-RADS
O sistema ACR TI-RADS classifica os nódulos tireoidianos com base em características ultrassonográficas, orientando a indicação de PAAF. [1] Cada característica ultrassonográfica recebe uma pontuação; a soma determina a categoria de risco e a conduta.

Pontuação por característica: [1][5]
Composição
Cístico ou quase completamente cístico: 0 pontos
Espongiforme (> 50% de espaços císticos): 0 pontos
Misto (cístico e sólido): 1 ponto; atribuir pontos conforme predominância sólida
Sólido ou quase completamente sólido: 2 pontos
Observação: considerar 2 pontos se a composição não foi determinada devido a calcificações
Ecogenicidade
Anecóico (aplicado a nódulos císticos ou quase císticos): 0 pontos
Hiperecóico ou isoecóico (comparação com parênquima): 1 ponto
Hipoecóico: 2 pontos
Muito hipoecóico (mais hipoecogênico que a musculatura): 3 pontos
Considerar 1 ponto se a ecogenicidade não foi determinada
Formato
Mais largo do que alto: 0 pontos
Mais alto do que largo (avaliado em imagem transversal com medidas paralelas ao feixe sonoro): 3 pontos
Margem
Regular ou bem definida: 0 pontos
Mal definida: 0 pontos [5]
Lobulada ou irregular: 2 pontos
Extensão extratireoidiana (invasão óbvia): 3 pontos
Considerar 0 pontos se a margem não foi determinada
Foco ecogênico
Nenhum ou rabo de cometa (artefato em V > 1 mm em componente cístico): 0 pontos
Macrocalcificações (causa sombra acústica): 1 ponto
Calcificações periféricas (completas ou incompletas ao longo da margem): 2 pontos
Foco puntiforme (pode apresentar pequenos artefatos em rabo de cometa): 3 pontos
Punção Aspirativa por Agulha Fina (PAAF)
A PAAF é o método mais acurado disponível para distinguir nódulos benignos dos malignos e constitui a pedra angular da avaliação do nódulo tireoidiano. [3][4] Trata-se de procedimento seguro, de baixo custo e com mínimas complicações sérias, que requer experiência tanto do executor quanto do citopatologista. [4]
Indicações: [1][3][4]
Todos os nódulos > 1 cm com função tireoidiana normal (eutiroidismo)
Nódulos ≤ 1 cm com características ultrassonográficas suspeitas ou história clínica de risco
Nódulos em bócio multinodular: os mesmos critérios se aplicam; se nenhum nódulo for suspeito ao US, aspirar o nódulo dominante [4]
PAAF guiada por US (situações preferenciais): [2][3]
Nódulos não palpáveis > 1 cm
Nódulos palpáveis < 1,5 cm
Nódulos profundos ou em proximidade a vasos
Lesões císticas ou mistas, especialmente após PAAF convencional não diagnóstica
Coexistência de linfadenopatia não palpável
Reduz significativamente a taxa de material insuficiente e aumenta a sensibilidade: de 91,8% para 97,1% [3]
Sensibilidade 100%, especificidade 80%, VPP 73%, VPN 100% [3]
Contraindicação: [1][4]
Nódulo hiperfuncionante (quente) confirmado à cintilografia — raramente maligno; PAAF contraindicada
Resultados da PAAF:
Os resultados da PAAF são classificados pelo Sistema Bethesda, que estratifica os achados citológicos em 6 categorias, cada uma associada a um risco estimado de malignidade e a uma conduta específica, detalhado no tópico abaixo.
Sistema Bethesda
O Sistema Bethesda para relato de citopatologia tireoidiana estratifica os resultados da PAAF em 6 categorias, orientando o risco de malignidade e a conduta subsequente. [1][2][5]
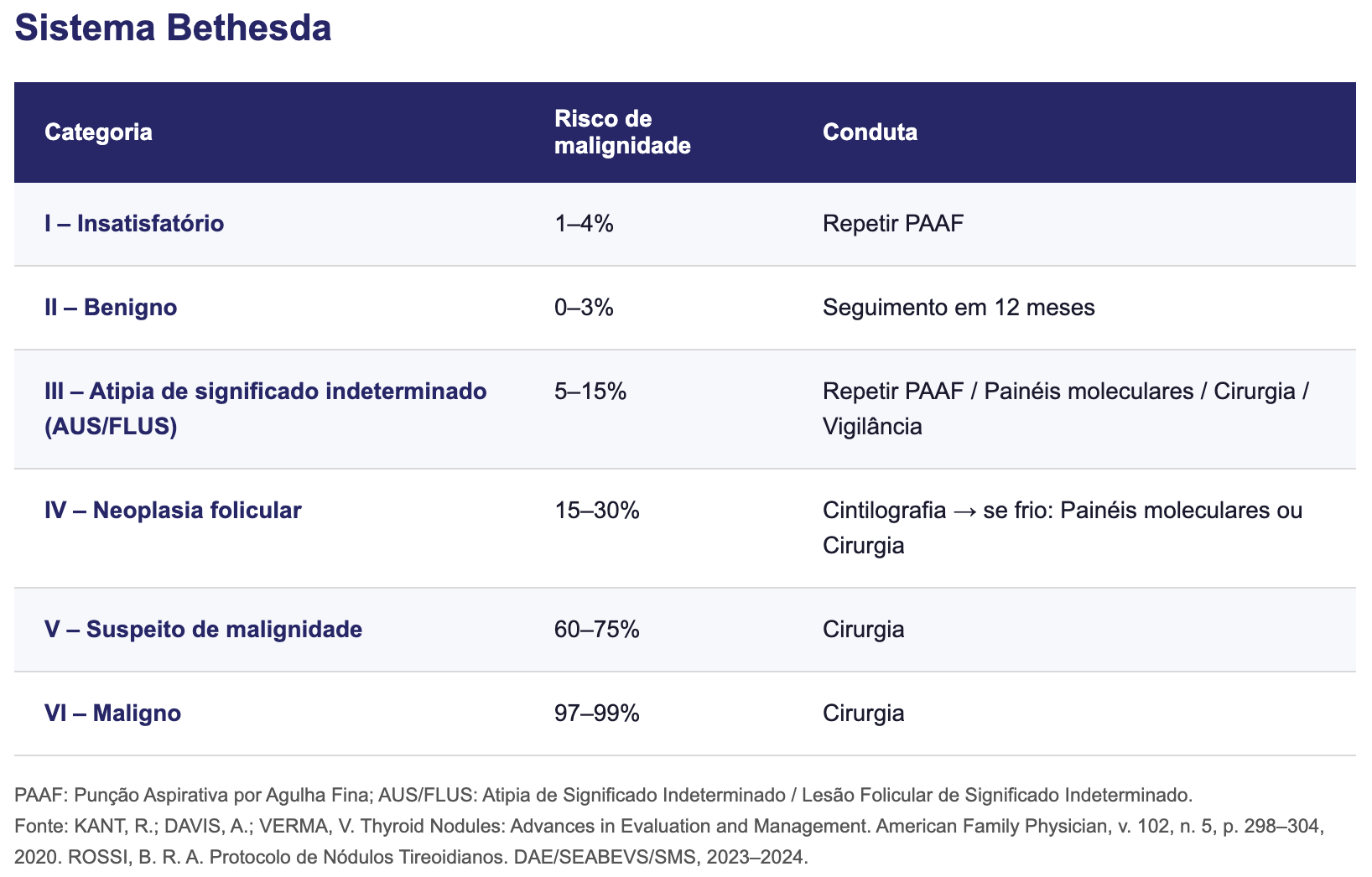
Detalhamento por categoria: [2][3][4][5]
Bethesda I (Insatisfatório)
Amostra citologicamente inadequada; ausência de células malignas não deve ser interpretada como biópsia negativa se o material for escasso [2]
Repetir PAAF guiada por US em 6–12 semanas [5]
Bethesda II (Benigno)
Inclui: nódulos colóides, bócio adenomatoso, bócio multinodular, tireoidite de Hashimoto, tireoidite granulomatosa subaguda [2]
Não requer cirurgia; seguimento ultrassonográfico periódico [2][4]
Bethesda III (Atipia de significado indeterminado — AUS/FLUS)
Lesões não convincentemente benignas com atipia nuclear ou padrão microfollicular/macrofollicular combinado [2]
A abordagem varia com a prática institucional: nova PAAF após 6–12 semanas [5], testes moleculares em material de PAAF ou vigilância ativa [2][5]
Testes moleculares: quando disponíveis, auxiliam na estratificação de risco e podem evitar cirurgias desnecessárias; um resultado benigno reduz significativamente o risco de malignidade, mas ainda requer seguimento por US [5]
Bethesda IV (Neoplasia folicular)
Inclui: adenomas microfolicularares ou celulares [2]
A distinção entre adenoma folicular benigno e carcinoma folicular (que difere apenas pela presença de invasão capsular ou vascular) é feita apenas pelo exame anatomopatológico da peça cirúrgica [2][3]
Indicar cintilografia: se nódulo quente, provável adenoma folicular, podendo dispensar cirurgia [3][4]
Se nódulo frio e testes moleculares não disponíveis: encaminhar para lobectomia diagnóstica [5]
Se nódulo frio com testes moleculares disponíveis: a conduta é orientada pelo resultado molecular [5]
Se lobectomia indicada: considerar tireoidectomia total em nódulos > 4 cm, bilaterais ou com alto risco [4]
Bethesda V (Suspeito de malignidade)
Lesões com características de malignidade não definitivas para câncer [2]
Indicação de cirurgia; encaminhamento para especialidade [2][5]
Bethesda VI (Maligno)
Inclui: carcinoma papilífero, carcinoma medular, linfoma tireoidiano, carcinoma anaplásico e metástases para a tireoide [2]
Indicação de cirurgia; encaminhamento imediato para especialidade [2][5]
Seguimento
Seguimento por categoria TI-RADS: [1][5]
TR 5 (altamente suspeito):
Nódulos ≥ 1 cm sem PAAF prévia: indicar PAAF [1]
Nódulos < 1 cm (abaixo do limiar de punção): repetir US em 6–9 meses; PAAF pode ser considerada em pacientes jovens ou por preferência do paciente [5]; exceto quando houver extensão extratireoidiana ou linfadenopatia cervical suspeita, situações em que a PAAF deve ser realizada independentemente do tamanho [5]
Nódulos TR5 com PAAF prévia benigna (Bethesda II) em acompanhamento: considerar repetir PAAF em 12 meses se a classificação TR5 persistir [1]
TR 3 ou 4 (suspeito leve a moderado):
Repetir US em 12 meses
Se estável: reavaliar em 3–5 anos
Se crescimento > 20% em diâmetro ou > 50% em volume, nova característica suspeita ou nova categoria de classificação: considerar PAAF e acompanhamento anual [1][5]
Seguimento de nódulos com Bethesda II (benigno): [2][4][5]
US periódica em 12–24 meses após PAAF inicial, com aumento progressivo dos intervalos se estável (podendo chegar a 3–5 anos) [2][5]
Repetir PAAF (preferencialmente guiada por US) se: [2][4][5]
Crescimento > 20% em pelo menos dois diâmetros ou > 50% em volume [2][5]
US apresentar achados altamente suspeitos, mesmo com biópsia inicial benigna
A vigilância anual é habitualmente adotada na prática; alterações entre exames podem modificar o intervalo conforme julgamento clínico [1]
Seguimento de nódulos ≤ 1 cm sem fatores de risco (incidentaloma de baixo risco): [3]
US periódica anual + controle da função tireoidiana (TSH) [3]
Reavaliação da indicação de PAAF caso surjam fatores de risco para malignidade [3]
Entre os pacientes com carcinoma papilífero < 1 cm em acompanhamento ultrassonográfico, 70% permanecem com o mesmo tamanho e apenas 10% apresentam aumento do diâmetro maior que 1 cm em 5 anos; o critério de monitorização do tamanho não é o principal fator para indicar PAAF nesse período [3]
⚠️ O tratamento supressivo com levotiroxina não é recomendado para nódulos benignos da tireoide, dado o risco de efeitos adversos cardiovasculares (fibrilação atrial em idosos) e ósseos (osteoporose em mulheres na pós-menopausa), sem benefício comprovado. [4][5]
Encaminhamento para Especialidade
Bethesda II (benigno): pode ser acompanhado pelo médico generalista [1]
Qualquer suspeita de malignidade: encaminhar para endocrinologia ou cirurgia de cabeça e pescoço [1]
Bethesda III, IV, V ou VI
Características clínicas ou ultrassonográficas de alto risco
Nódulo hiperfuncionante confirmado (para avaliação de tratamento específico) [1]
Quando confirmada a malignidade:
A extensão da ressecção cirúrgica, sendo lobectomia ou tireoidectomia total, é definida pelo cirurgião de cabeça e pescoço com base no risco individual do paciente.
A lobectomia é aceitável em tumores papilíferos de baixo risco (< 4 cm, unifocais, sem extensão extratireoidiana ou comprometimento linfonodal); a tireoidectomia total é preferencial em tumores > 4 cm, bilaterais, com extensão extratireoidiana, comprometimento linfonodal ou metástase à distância. [4][5]
O manejo pós-cirúrgico, incluindo radioiodoterapia (¹³¹I), supressão de TSH com levotiroxina e seguimento com tireoglobulina sérica, é de competência do endocrinologista. [4]
Referências
[1] ROSSI, Beatriz R. A. Protocolo de Nódulos Tireoidianos. Departamento de Atenção Especializada (DAE); Secretaria Executiva de Atenção Básica, Especialidades e Vigilância em Saúde (SEABEVS); Secretaria Municipal da Saúde (SMS). 2023–2024.
[2] ZAMORA, Edgar A.; KHARE, Swapnil; CASSARO, Sebastiano. Thyroid Nodule. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2026. Última atualização: 4 set. 2023. Disponível em: https://www.ncbi.nlm.nih.gov/books/NBK535422/. Acesso em: 11 abr. 2026.
[3] KIMURA, E. T. et al. Doença Nodular da Tireoide: Diagnóstico. Diretrizes Clínicas na Saúde Suplementar. Associação Médica Brasileira e Agência Nacional de Saúde Suplementar. Autoria: Sociedade Brasileira de Endocrinologia e Metabolismo; Sociedade Brasileira de Cirurgia de Cabeça e Pescoço; Sociedade Brasileira de Citopatologia. Elaboração final: 31 jan. 2011. Disponível em: https://www.ans.gov.br.
[4] MAIA, Ana Luiza et al. Nódulos de Tireóide e Câncer Diferenciado de Tireóide: Consenso Brasileiro. Arquivos Brasileiros de Endocrinologia e Metabologia, v. 51, n. 5, p. 867–893, 2007. Pelo Departamento de Tireóide, Sociedade Brasileira de Endocrinologia e Metabologia. Disponível em: https://www.sbem.org.br.
[5] KANT, Ravi; DAVIS, Amanda; VERMA, Vipin. Thyroid Nodules: Advances in Evaluation and Management. American Family Physician, v. 102, n. 5, p. 298–304, set. 2020. Disponível em: https://www.aafp.org/afp/2020/0901/p298.html.
Autoria e Curadoria
As informações contidas nesta página são de autoria da Equipe Editorial Médica do GPMED, composta por médicos especialistas de diversas áreas. Todo o conteúdo é estruturado rigorosamente com base em fontes bibliográficas de alto impacto e nas diretrizes oficiais vigentes, seguindo os preceitos da Medicina Baseada em Evidências. Nosso compromisso é oferecer ao médico uma base de consulta técnica, confiável e chancelada por profissionais experientes, garantindo máxima segurança no suporte à decisão clínica.


